
(7分)用下面的装置将一定量的CO2和CO的混合气体进行分离和干燥。图中的a、b、c、d均为活塞,可以控制气体的通过和液体的加入,实验前活塞均已关闭。请选择适宜的试剂完成上述实验。(仪器的固定装置已经省略) 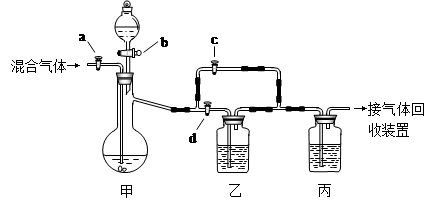
可供选择的试剂有:①浓硫酸 ②稀硫酸 ③浓盐酸
④稀盐酸 ⑤澄清的石灰水 ⑥氢氧化钠溶液
实验分以下两步进行:(所选的试剂均用序号表示)
⑴关闭b、c,打开a、d,则甲中试剂为 ,丙中试剂为 。若乙装置中的现象是 ,说明甲装置中反应是充分的。此步实验后收集到的气体是 。
⑵在甲装置的分液漏斗中加入试剂②或④,关闭活塞 (填写序号,下同),打开活塞 ,再经过丙装置后即可收集到另一种气体。此步实验中发生的反应方程式为 。
⑴⑥ ① 溶液不变浑浊(答案合理就即可) CO ⑵ a、d b、c Na2CO3+2HCl="=2NaCl+" H2O+ CO2↑ 或:Na2CO3+H2SO4= Na2SO4+H2O+CO2↑
解析试题分析:(1)要用题中装置将一定量的CO2和CO的混合气体进行分离和干燥,先用氢氧化钠把二氧化碳反应掉,乙装置是用来检验第一步是不是已经把二氧化碳彻底吸收掉了,这样才会在装置后得到一氧化碳。关闭b、c,打开a、d,则甲中试剂为⑥氢氧化钠溶液,丙中试剂为①浓硫酸。若乙装置中的现象是溶液不变浑浊,说明甲装置中反应是充分的。此步实验后收集到的气体是CO;
(2)在甲装置的分液漏斗中加入试剂②或④,关闭活塞a、d ;打开活塞b、c;则加入的稀硫酸或稀盐酸将与上一步反应生成的碳酸钠反应,生成二氧化碳气体,再经过丙装置后即可收集到二氧化碳。此步实验中发生的反应方程式为:Na2CO3+2HCl="=2NaCl+" H2O+ CO2↑ 或:Na2CO3+H2SO4= Na2SO4+H2O+CO2↑
考点:混合物的分离;气体的干燥;二氧化碳的性质;一氧化碳的性质;书写化学方程式。
点评:本题考查分离一氧化碳与二氧化碳,题中是先用试剂将二氧化碳吸收得到一氧化碳,再通过试剂反应,得到二氧化碳的。


科目:初中化学 来源: 题型:阅读理解
| MnO2 |
| MnO2 |
| 加热 |
| 加热 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 二氧化锰 |
| 二氧化锰 |
| 加热 |
| 加热 |
| 二氧化锰 |
| 加热 |
| 二氧化锰 |
| 加热 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解


| 加热 |
| 加热 |
查看答案和解析>>
科目:初中化学 来源:2010届北京市东城区中考一模化学试卷(解析版) 题型:探究题
(7分)用下面的装置将一定量的CO2和CO的混合气体进行分离和干燥。图中的a、b、c、d均为活塞,可以控制气体的通过和液体的加入,实验前活塞均已关闭。请选择适宜的试剂完成上述实验。(仪器的固定装置已经省略)
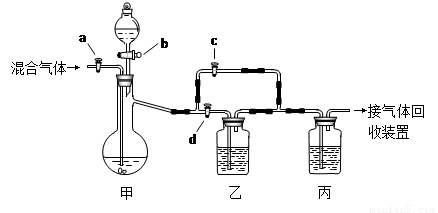
可供选择的试剂有:①浓硫酸 ②稀硫酸 ③浓盐酸
④稀盐酸 ⑤澄清的石灰水 ⑥氢氧化钠溶液
实验分以下两步进行:(所选的试剂均用序号表示)
⑴ 关闭b、c,打开a、d,则甲中试剂为 ,丙中试剂为 。若乙装置中的现象是 ,说明甲装置中反应是充分的。 此步实验后收集到的气体是 。
⑵ 在甲装置的分液漏斗中加入试剂②或④,关闭活塞 (填写序号,下同),打开活塞 ,再经过丙装置后即可收集到另一种气体。此步实验中发生的反应方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com