
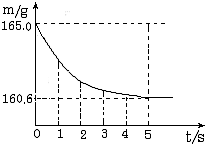
 (2005?镇江)在烧杯中加入氯化钠和碳酸氢钠的固体混合物10.0g后,再加入68.9g稀盐酸恰好完全反应.反应过程用精密仪器测得烧杯连同药品的总质量(m)与反应时间(t)的关系如图所示.烧杯连同药品的起始总质量为165.0g.反应的方程式为:NaHCO3+HCl═NaCl+H2O+CO2↑试回答下列问题:
(2005?镇江)在烧杯中加入氯化钠和碳酸氢钠的固体混合物10.0g后,再加入68.9g稀盐酸恰好完全反应.反应过程用精密仪器测得烧杯连同药品的总质量(m)与反应时间(t)的关系如图所示.烧杯连同药品的起始总质量为165.0g.反应的方程式为:NaHCO3+HCl═NaCl+H2O+CO2↑试回答下列问题:| 混合物中氯化钠的质量+生成氯化钠质量 |
| 反应后所得溶液的质量 |
| 84 |
| x |
| 58.5 |
| y |
| 44 |
| 4.4g |
| 5.85g+1.6g |
| 74.5g |


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com