
 2yH2O+4xCO2+2N2,依据依据质量守恒定律以及该反应的方程式结合提供的数值分析解答即可;
2yH2O+4xCO2+2N2,依据依据质量守恒定律以及该反应的方程式结合提供的数值分析解答即可;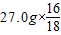 +
+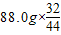 =88g,因此生成的氮气质量应为29.8g+88g-27.0g-88.0g=2.8g.
=88g,因此生成的氮气质量应为29.8g+88g-27.0g-88.0g=2.8g.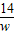 ×100%=
×100%=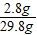 ×100%
×100%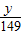 =27.0g×
=27.0g×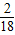
 2yH2O+4xCO2+2N2结合质量守恒定律可知生成物中的氧元素应该与反应的氧气的质量相等,
2yH2O+4xCO2+2N2结合质量守恒定律可知生成物中的氧元素应该与反应的氧气的质量相等, +
+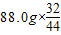 =88g,因此生成的氮气质量应为29.8g+88g-27.0g-88.0g=2.8g.
=88g,因此生成的氮气质量应为29.8g+88g-27.0g-88.0g=2.8g. 2yH2O+4xCO2+2N2
2yH2O+4xCO2+2N2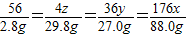


 口算能手系列答案
口算能手系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:黑龙江省中考真题 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:
冰毒是毒品“摇头丸”的主要成分,具有强烈的致幻效果,易成瘾,对吸食者造成严重的伤害。它的分子式为CxHyN,取29.8g冰毒充分燃烧生成27.0g H2O,88.0g CO2和一定质量的N2,试求(写出计算过程)
(1)冰毒的相对分子质量;
(2)求X,Y的值。
查看答案和解析>>
科目:初中化学 来源:中考化学试题分类卷(三)(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com