
| A. | 燃放鞭炮 | B. | 城市绿化 | C. | 露天焚烧垃圾 | D. | 工厂排放烟尘 |
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:初中化学 来源: 题型:选择题
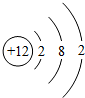 某元素的一种粒子的结构示意图如图所示,下列对该粒子的判断中,错误的是( )
某元素的一种粒子的结构示意图如图所示,下列对该粒子的判断中,错误的是( )| A. | 该粒子是金属元素的原子 | |
| B. | 该元素在化合物中显-2价 | |
| C. | 该元素1个原子的原子核内有12个质子 | |
| D. | 该元素的原子在化学反应中容易失去电子 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | / | |
| ② | 1.2g | CuO 0.5g | |
| ③ | 1.2g | MnO2 0.5g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
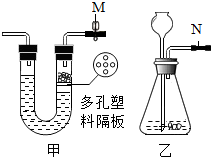
| A. | 此时甲装置中的止水夹M处于关闭状态 | |
| B. | 甲装置具有控制反应的开始与结束的功能 | |
| C. | 乙装置的长颈漏斗下端一定要伸入液体中起液封作用 | |
| D. | 乙装置N处添加止水夹可以与甲装置具有相同功能 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
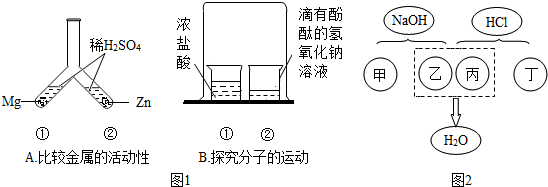
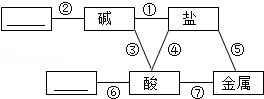 归纳是学习化学的重要方法,总结出如图所示的物质之间的反应关系(图中短线连接的物质表示能相互反应),请帮助完成下列空白:
归纳是学习化学的重要方法,总结出如图所示的物质之间的反应关系(图中短线连接的物质表示能相互反应),请帮助完成下列空白:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
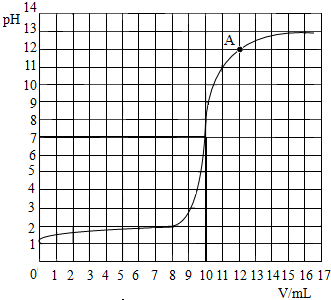 在盛有10克稀盐酸的烧杯中,逐滴滴加溶质质量分数为4%的氢氧化钠溶液,反应过程中不断搅拌并及时用pH计(一种测定溶液pH的仪器)测定溶液的pH,烧杯中溶液的pH与加入氢氧化钠溶液体积(V)之间的变化关系如图所示.
在盛有10克稀盐酸的烧杯中,逐滴滴加溶质质量分数为4%的氢氧化钠溶液,反应过程中不断搅拌并及时用pH计(一种测定溶液pH的仪器)测定溶液的pH,烧杯中溶液的pH与加入氢氧化钠溶液体积(V)之间的变化关系如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com