
| A. | 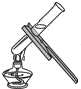 给液体加热 | B. | 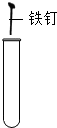 放入铁钉 | C. | 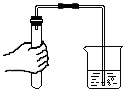 检查气密性 | D. | 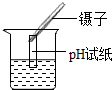 测溶液的酸碱度 |
分析 A、根据给试管中的液体加热的方法进行分析判断;
B、根据固体药品的取用方法进行分析判断;
C、根据检查装置气密性的方法进行分析判断;
D、根据用pH试纸测定液体的酸碱度进行分析.
解答 解:A、给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的$\frac{1}{3}$,试管夹应夹在距试管口大约$\frac{1}{3}$处,大拇指不能放在短柄上,图中所示操作错误;
B、向试管中加入固体药品时,应先将试管横放,用镊子把铁钉放在试管口,再慢慢将试管竖立起来,图中所示操作错误;
C、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气;图中所示操作正确;
D、用pH试纸测定液体的酸碱度时,要用滴管将液体滴加到干燥的试纸上,不能把试纸直接插入待测液体中,故操作错误;
故选C.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 观察NaCl、CaCl2溶液的颜色 | |
| B. | 观察Fe2(SO4)3、Fe(NO3)3溶液的颜色 | |
| C. | FeCl3溶液中滴加适量的NaOH溶液,静置后观察溶液的颜色 | |
| D. | 加水稀释后观察颜色 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 13 | B. | 14 | C. | 18 | D. | 27 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 温度/℃ | 0 | 20 | 40 | 60 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 化学式 | 颜色状态 | 酸碱性 | 加热 | 滴加稀盐酸 | 滴加硝酸银溶液 |
| NaCl | 白色固体 | 中性 | 受热不分解 | 无明显变化 | 生成白色沉淀 |
| NaNO2 | 白色固体 | 弱碱性 | 320℃以上分解生成刺激性气味的气体 | 生成红棕色气体 | 无明显变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
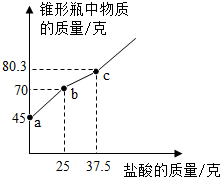 为测定某氢氧化钙(只含有碳酸钙杂质)样品的变质程度,称取研细的该样品12.4g放入锥形瓶中,加入32.6g水,充分振荡形成悬浊液,再向锥形瓶中逐滴滴加盐酸使其充分反应至无气泡产生,测得加入盐酸的质量与锥形瓶中物质的质量关系如图所示.
为测定某氢氧化钙(只含有碳酸钙杂质)样品的变质程度,称取研细的该样品12.4g放入锥形瓶中,加入32.6g水,充分振荡形成悬浊液,再向锥形瓶中逐滴滴加盐酸使其充分反应至无气泡产生,测得加入盐酸的质量与锥形瓶中物质的质量关系如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com