
【题目】某化学兴趣小组通过探究活动学习和理解化学知识.请你一起研究学习,并回答有关问题.
研究主题:水溶液中复分解反应的实质
相关信息:一定体积的溶液中,离子的数目越多,其离子的浓度越大.电导率传感器用于测量溶液的导电性强弱,能反映离子浓度大小.相同温度下同种溶液电导率越大,离子浓度越大.
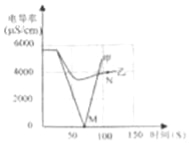
(1)实验一:恒温条件下,向一定体积一定浓度的稀Ba(OH)2溶液中滴加2﹣3滴无色酚酞试液,插入电导率传感器,然后滴加稀硫酸,测得溶液的电导率变化如图中甲曲线所示.
①写出Ba(OH)2与H2SO4反应的化学方程式 .
②甲曲线M点时混合液体呈 色;
③通过对甲曲线的分析,下列说法错误的是 (填序号).
A.M点前曲线下滑的过程中,H+和OH﹣结合成H2O,Ba2+和SO42﹣结合成BaSO4
B.M点时离子浓度几乎为零 C.M点后溶液电导率逐渐增大,仅由于溶液中H+在逐渐增大
(2)实验二:恒温条件下,向等量同浓度的稀Ba(OH)2溶液中滴加2﹣3滴无色酚酞试液,插入电导率传感器,然后滴加稀Na2SO4溶液,测得溶液的电导率变化如上图乙曲线所示.
①通过对乙曲线的分析,下列说法错误的是 (填序号).
A.开始至完全反应过程中,电导率减小,溶液由红色逐渐变为无色
B.电导率下降到最低点时仍然较大,表明溶液中还存在较多离子
C.整个实验过程中,溶液中Na+数目一直增大
②N点时,溶液中含有的离子是 (填离子符号).
③通过比较分析,结合已学知识可知,溶液中复分解反应的实质是参与反应的离子,结合生成了沉淀、气体或水,导致其浓度 (填“增大”或“减小”).
(3)拓展:①请根据示例仿写离子方程式.
示例AgNO3+NaCl=AgCl↓+NaNO3离子方程式:Ag++Cl﹣=AgCl↓
仿写:BaCl2+Na2SO4=BaSO4↓+2NaCl离子方程式: .
②向一定量饱和澄清石灰水中持续通入过量的CO2气体,溶液先变浑浊后浑浊逐渐消失.请推测此过程的溶液中Ca2+的浓度变化情况 .
【答案】(1)Ba(OH)2+H2SO4=BaSO4↓+2H2O.;无; C;
(2)A; Na+、OH﹣、SO42﹣;减小.(3)Ba2++SO42﹣=BaSO4↓.先减小后增大.
【解析】(1)①Ba(OH)2与H2SO4反应生成硫酸钡沉淀和水,反应的化学方程式为Ba(OH)2+H2SO4=BaSO4↓+2H2O,②甲曲线M点时二者恰好完全反应,溶液呈中性,酚酞为无色,故混合液体呈无色,③A.M点前曲线下滑的过程中,H+和OH﹣结合成H2O,Ba2+和SO42﹣结合成BaSO4,正确;B.M点时二者恰好完全反应,离子浓度几乎为零,正确;C.M点后溶液电导率逐渐增大,不仅由于溶液中H+在逐渐增大,硫酸根离子也在增大,错误;(2)①A.开始至完全反应过程中,电导率减小,反应生成的氢氧化钠呈碱性,溶液仍为红色,错误;B.电导率下降到最低点时仍然较大,表明溶液中还存在较多离子,正确;C.整个实验过程中,溶液中Na+数目一直增大,正确;②N点时,溶液中含有氢氧化钠和过量的硫酸钠,故含有的离子是钠离子、氢氧根离子和硫酸根离子。③溶液中复分解反应的实质是参与反应的离子,结合生成了沉淀、气体或水,导致其浓度减小。(3)①BaCl2+Na2SO4=BaSO4↓+2NaCl反应的实质是钡离子和硫酸根离子结合产生硫酸钡沉淀,其离子方程式为Ba2++SO42﹣=BaSO4↓;②向一定量饱和澄清石灰水中持续通入过量的CO2气体,溶液先变浑浊,此过程中钙离子浓度逐渐减小,浑浊逐渐消失的过程中钙离子的浓度逐渐增大。


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:初中化学 来源: 题型:
【题目】硼氢化钠【化学式(NaBH4)】,是一种安全车载氢源。
(l)硼氢化钠中Na、B、H元素的质最比为_______(最简整数比);
(2)硼氢化钠中氢元素的化合价为-1价,硼元素的化合价为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一定条件下,一个密闭容器内发生某反应,测得反应过程中各物质的质量部分数据如下表所示:
物质 | 甲 | 乙 | 丙 | 丁 |
反应前的质量/g | 12 | 26 | 3 | 0 |
反应中的质量/g | 9 | 22 | 3 | b |
反应后的质量/g | 0 | a | 3 | 28 |
下列说法正确的是( )
A.a等于10 B.该化学反应为复分解反应 C.丙一定为催化剂 D.b等于12
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )
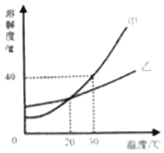
A.30℃时,甲的饱和溶液溶质质量分数为40%
B.20℃时,甲、乙的饱和溶液中所含溶质的质量一定相等
C.将等质量的甲、乙固体,分别配成30℃的饱和溶液,所需水的质量:甲>乙
D.将20℃时甲、乙的饱和溶液升温到30℃,所得甲、乙溶液的溶质质量分数相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下列装置回答问题。

(1)写出A图中标号① 的仪器名称________。
(2)用过氧化氢溶液和二氧化锰制取氧气.选择的发生装置是______(填装置序号);现准备收集一瓶氧气供铁丝燃烧的实验使用,选择______(填装置序号)装置收集氧气便于直接做这个实验;
(3)某同学利用空塑料输液袋(如图F)收集二氧化碳,验满二氧化碳时,把说着的火柴放在玻璃管_____(填“a”或“b”)端,如果火焰熄火.则收集满了。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碱式碳酸镁[Mg2(OH)2CO3]和过氧化镁(MgO2)都是重要化工原料。
Ⅰ 以Mg2(OH)2CO3为原料,制备产品MgO2的步骤如下:
(1)煅烧 煅烧Mg2(OH)2CO3得到三种氧化物,其中一种常温下是气体,且能使澄清石灰水变浑浊。煅烧时反应的化学方程式为 。
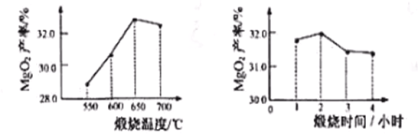
(2)转化 向所得固体中加双氧水充分搅拌,发生反应MgO+H2O2=MgO2+H2O。温度升高,说明该反应 热量(填“放出”或“吸收”)。其他条件相同,煅烧温度、煅烧时间不同,所得MgO对MgO2产率(产率=![]() ×100%)的影响分别如图所示。则最佳的煅烧温度为 ℃,煅烧时间为 小时。
×100%)的影响分别如图所示。则最佳的煅烧温度为 ℃,煅烧时间为 小时。
(3)分离 得到产品
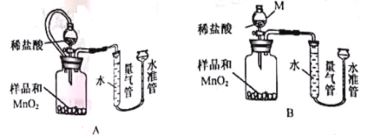
(4)测定 假设产品中仅混有少量MnO。某小组设计下列装置,通过测定生成O2的体积,计算MgO2的质量分数。
已知:A.MnO2与稀盐酸不反应 B.MgO2+2HCl=MgCl2+H2O2
C.2MgO2![]() 2MnO+O2↑ D.MgO+C
2MnO+O2↑ D.MgO+C![]() Mg+CO↑
Mg+CO↑
①仪器M的名称是 。MnO2的作用是 。
②相同条件下, 能使测定结果更准确。(填“装置A”或“装置B”)
③实验室用溶质质量分数为37%、密度是1.18g·mL-1的浓盐酸配制10%的稀盐酸110g,需要水 mL。(水的密度是1g·mL-1,计算结果保留一位小数)
④经讨论,该小组又设计了下列3种方案。分别取5.0g产品进行实验,能确定MgO2质量分数的是 。(填序号)
A.加热,使MgO2完全分解,测出剩余固体的质量
B.与足量炭粉在高温下充分反应,测出生成Mg的质量
C.先加足量稀盐酸,再加足量NaOH溶液,充分反应,测出Mg(OH)2质量
Ⅱ MgCl2是制备Mg2(OH)2CO3的原料。现用含碳酸镁84%的菱镁矿制备MgCl2,反应如下:
MgCO3+Cl2+CO![]() MgCl2+2CO2(设杂质不参加反应)。生产19吨MgCl2需要这样的菱镁矿多少吨?(写出计算过程)
MgCl2+2CO2(设杂质不参加反应)。生产19吨MgCl2需要这样的菱镁矿多少吨?(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是元素周期表中1-18号元素的原子结构示意图,请回答下列问题:
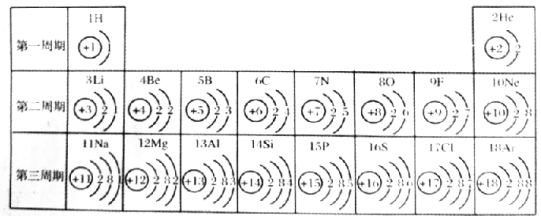
(l)原子序数为17的元素属于______(填“金属”或“非金属”)元素。表中与该元素化学性质相似的元素是_______(填元素名称)。
(2)X3-和氖原子的核外电子排布相同,则X的元素符号是______。
(3)同一周期,从左到右,各元素原子的______依次递增。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com