
| 1 |
| x |
| 1 |
| 0.1mol |
| 10g |
| 12.5g |


科目:初中化学 来源: 题型:
A、2CO+O2
| ||||
B、2HgO
| ||||
C、2Al2O3
| ||||
D、CaCO3
|
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、Cu Ag |
| B、Zn Fe |
| C、Cu Pt |
| D、Ag Au |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
| Ca(OH)2 | 0.18 | 0.16 | 0.14 | 0.12 | 0.09 | 0.07 | |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、刚好成为饱和溶液 |
| B、仍为不饱和溶液 |
| C、为饱和溶液并有晶体析出 |
| D、为不饱和溶液并有晶体析出 |
查看答案和解析>>
科目:初中化学 来源: 题型:
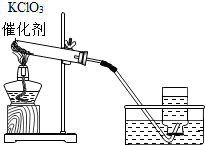 在实验室中用MnO2做为KClO3分解制氧气的催化剂:2KClO3
在实验室中用MnO2做为KClO3分解制氧气的催化剂:2KClO3
| ||
| △ |
| 实验组别 | KClO3质量(克) | 催化剂 | 产生气体质量(克) | 耗时(秒) | |
| 化学式 | 质量(克) | ||||
| 1 | 0.60 | - | - | 0.014 | 480 |
| 2 | 0.60 | MnO2 | 0.20 | 0.096 | 36.5 |
| 3 | 0.60 | CuO | 0.20 | 0.096 | 79.5 |
| 4 | 0.60 | Fe2O3 | 0.20 | 0.096 | 34.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com