
| A. |  闻气味 | B. | 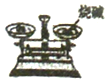 称量固体 | C. |  滴加液体 | D. | 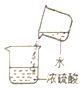 稀释浓硫酸 |
分析 A、根据闻气体的气味时的方法(招气入鼻法)进行分析判断.
B、根据托盘天平的使用要遵循“左物右码”的原则进行分析判断.
C、根据使用胶头滴管滴加少量液体的方法进行分析判断.
D、根据浓硫酸的稀释方法(酸入水,沿器壁,慢慢倒,不断搅)进行分析判断.
解答 解:A、闻气体的气味时,应用手在瓶口轻轻的扇动,使极少量的气体飘进鼻子中,不能将鼻子凑到集气瓶口去闻气体的气味,图中所示操作正确.
B、托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,图中所示操作错误.
C、使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到试管内或接触试管内壁,应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图中所示操作错误.
D、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中;图中所示操作错误.
故选:A.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:初中化学 来源: 题型:选择题
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
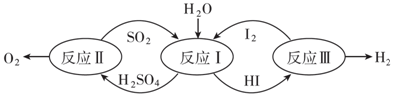
| A. | 反应Ⅰ方程式为:SO2+I2+2H2O=H2SO4+2HI | |
| B. | 反应Ⅱ中的第二步反应中,SO3分解生成S和O2 | |
| C. | 反应Ⅰ属于化合反应,反应Ⅱ、III属于分解反应 | |
| D. | 该生产工艺中最终被消耗的物质是H2O、S和I2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 毛织品和棉织品-点燃少许样品并闻气味 | |
| B. | 钾肥和铵态氮肥-加熟石灰研磨,闻气味 | |
| C. | 氢气、一氧化碳-通入灼热的氧化铜,看固体颜色变化 | |
| D. | 黄金和黄铜(铜锌合金)-加入稀盐酸中,观察是否有气泡产生 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
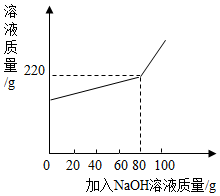 将一定量氯化镁和氯化钠的固体混合物加水配成145.8g的溶液,向所得溶液中加入一定浓度的氢氧化钠溶液,加入氢氧化钠溶液的质量与反应后溶液的质量关系如图.计算:
将一定量氯化镁和氯化钠的固体混合物加水配成145.8g的溶液,向所得溶液中加入一定浓度的氢氧化钠溶液,加入氢氧化钠溶液的质量与反应后溶液的质量关系如图.计算:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用氢氧化钙治疗胃酸过多 | |
| B. | 用硫酸钡作胃部 X 光检查时服用的“钡餐” | |
| C. | 用食醋除去水瓶中的水垢 | |
| D. | 用铅笔芯的粉末使锁的开启变得更灵活 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
| 取一定量纯碱样品配成溶液后,滴加过量的CaCl2溶液. | 产生白色沉淀 | 反应的化学方程式: Na2CO3+CaCl2═CaCO3↓+2NaCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com