
【题目】t℃时,测得某物质(不含结晶水)在不同质量的水中溶解,达到饱和状态时所溶解该物质的质量,绘制成如图中斜线。下列说法正确是
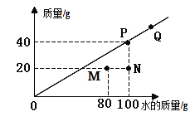
A.该物质的溶解度随温度的升高而增大
B.t℃时该物质的溶解度为40
C.M点表示溶液中溶质的质量分数为25%
D.图中4点表示的溶液中溶质质量分数的关系是:N<M<P=Q
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案科目:初中化学 来源: 题型:
【题目】(11分)已知过氧化钠(化学式为Na2O2)是一种浅黄色固体粉末,可用作呼吸面具里的供氧剂,利用人呼出的二氧化碳与Na2O2反应放出O2,供给人的正常生命活动,该反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2。某同学利用该反应原理制取氧气,设计了如图一所示的实验装置。
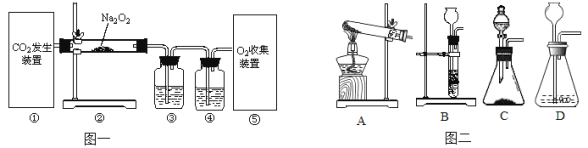
(1)装置①中CO2的制取方法有多种,若用稀盐酸和石灰石制取CO2,该反应的化学方程式为 。若用加热NaHCO3固体制取CO2,应该选用的发生装置为 (选填图二中字母)。
(2)夏天室温很高的时候,检验A装置气密性的合理方法是:将导管口放入水面下,然后 ,若导管口有气泡冒出……,说明装置不漏气。
(3)为收集纯净干燥的O2,装置③中盛放的试剂为 ,作用是 ;装置④中盛放的试剂为 ,作用是 ;则⑤中收集方法可选用 。
A.排水集气法 B.向下排空气法
C.向上排空气法 D.真空袋收集法
(4)当观察到装置②中 时应停止通CO2。
(5)此外,过氧化钠也能与水反应生成碱和氧气, 试写出该反应的化学方程式 ,若用此反应制O2,可选用的发生装置为 (选填图二中字母)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】草酸是一种酸,草酸晶体(H2C2O42H2O)易溶于水,熔点较低,加热会熔化、气化和分解。草酸(H2C2O4)与氢氧化钙的反应:H2C2O4 + Ca(OH)2= CaC2O4↓(白色)+ 2H2O。
【分析讨论】
(1)草酸的水溶液的pH 7(填“>”、“=”、“<”)
(2)实验室可用加热草酸晶体分解的方法获得CO
①先加热草酸晶体生成CO、CO2和H2O,其化学方程式是 ;
②再将生成的混合气体通过NaOH溶液吸收CO2,其化学方程式是 ;
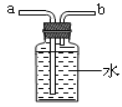
③最后用下图装置收集CO,气体应从 端进入(选填“a”或“b”)。
【实验反思】
(3)甲认为下图中试管口应略向下倾斜,老师、同学讨论后一致认为装置是正确的,理由是 。
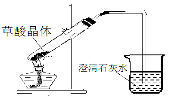
(4)实验中观察到澄清石灰水变浑浊,乙认为一定是由草酸晶体受热分解产生的CO2所导致,丙认为乙的结论不严密,理由是 。
【生活链接】菠菜营养丰富,但菠菜豆腐同食,易得结石(主要成分:草酸钙晶体),小组同学对草酸钙晶体的性质及组成产生了兴趣。
【性质探究】按下图装置将草酸钙晶体(CaC2O4·xH2O)样品高温加热,使其完全分解并检验产生的气体。
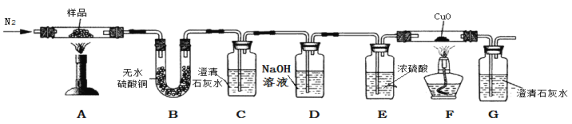
【问题讨论】
(5)B中观察到 现象,说明反应生成了水;
(6)C、G中澄清石灰水均变浑浊,说明反应还生成 和 气体。
(7)反应开始前通入氮气的目的是 。
【组成确定】
(8)利用热分析仪对草酸钙晶体(CaC2O4·xH2O)进行热分解,获得相关数据,绘制成固体质量—分解温度的关系如图。
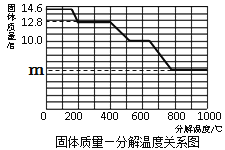
①温度为200℃左右时,晶体全部失去结晶水,晶体中结晶水的质量为 g。
②计算CaC2O4·xH2O中的x(CaC2O4的相对分子质量:128),x = 。
③800℃以上时,经检验残留固体为氧化物,图中m的值是 。
④写出固体质量由12.8g变为10.0g时的化学方程式 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法不正确的是
A.敞口放置的浓硫酸,放置过程中,溶质质量分数会减小
B.通过相互刻划的方法,发现黄铜片的硬度比铜片大
C.鉴别碘和高锰酸钾,可分别取少量加入水中并振荡,然后观察现象
D.化学反应常常伴随着能量变化,因此有能量释放的变化都是化学反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(6分)我县自来水的处理过程如图所示:
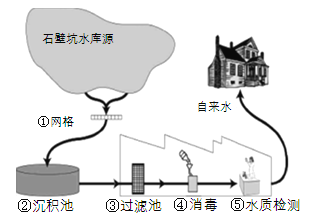
(1)步骤①网格净水原理类似于 操作;
(2)步骤②所起的作用是 (填序号);
A.杀死水中的细菌 B.加快过滤速度
C.使泥沙沉积至底部 D.分解有毒物质
(3)步骤④中的消毒剂除氯气以外,还可用一氯胺(NH2Cl)、二氧化氯等物质。
①二氧化氯的化学式为 。
②NH2Cl中氮、氢、氯三种元素的质量比是 (结果以最简整数比表示)。
(4)生活中将自来水软化的常用方法是 ,区分软水和硬水的试剂是_______ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关空气各成分的说法正确的是:
A、氧气的化学性质比较活泼,属于可燃物
B、氮气的化学性质不活泼,可用于食品防腐
C、空气质量报告中所列的空气质量级别越大,空气质量越好
D、二氧化碳在空气中含量增多会引起温室效应,属于空气污染物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(4分)水是生命之源,通过化学学习,我们进一步认识到水的重要作用。
(1)自然界的水常遭到污染,污染物中氮和磷含量过高会造成“赤潮”或“水华”现象。这里的“氮和磷”是指 (填字母)
A.元素 B.原子 C.离子 D.分子
(2)自然界的水硬度较高,需要经过:①煮沸 ②消毒 ③过滤 ④自然沉降等净化过程,其中处理顺序合理的是 (填序号)。自来水因含杂质不是纯水,若要制取纯水,应采取的净化方法是 。
(3)高铁酸钾(K2FeO4)是一种新型、高效的多功能水处理剂。高铁酸钾受热时发生的反应为:
4K2FeO4![]() 2R+4K2O+3O2↑,则R是 (填化学式)。
2R+4K2O+3O2↑,则R是 (填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com