
| 实验操作 | 实验现象 | 实验结论 |
| 将步骤三B试管中溶液倒入盛有锌粒的试管中 | 有气泡产生 | 猜想一正确 |
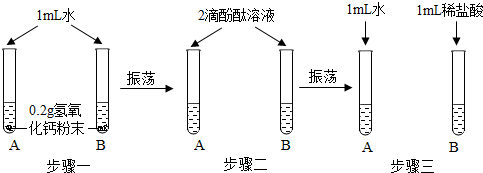
分析 (1)氢氧化钙溶液显碱性能使酚酞变红色;
(2)【猜想】根据反应的情况分析;
【小组讨论】相互反应的物质不能共存;
【实验探究】根据活泼金属和酸反应放出氢气进行分析;
【讨论交流】根据实验探究可知所做的实验结束后,试管中所得溶液一定含有的溶质是氯化钙和氯化锌进行解答.
解答 解:(1)氢氧化钙溶液显碱性能使酚酞变红色;说明A试管的水中溶有氢氧化钙的现象是步骤二中的A试管变红色;
(2)【猜想】氧化钙与水反应生成氢氧化钙,氢氧化钙与盐酸反应后溶液澄清并无色,说明盐酸过量或恰好反应,除指示剂外,溶质的成分还有CaCl2、HCl或只有CaCl2;
【小组讨论】相互反应的物质不能共存,Ca(OH)与HCl会发生反应,所以Ca(OH)与HCl不能共存;
【实验探究】根据活泼金属和酸反应放出氢气进行分析.所以将步骤三B试管中溶液倒入盛有锌粒的试管中,有气泡冒出,说明猜想一正确;
| 实验操作 | 实验现象 | 实验结论 |
| 将步骤三B试管中溶液倒入盛有锌粒的试管中 | 有气泡产生 | 猜想一正确 |
| 实验操作 | 实验现象 | 实验结论 |
| 将步骤三B试管中溶液倒入盛有锌粒的试管中 | 有气泡产生 | 猜想一正确 |
点评 本题要求学生牢固掌握有关酸碱的知识,才能正确解答.同时检查学生从实验中获取信息的能力.


科目:初中化学 来源: 题型:选择题
| A. | 添加适量铁元素的酱油 | B. | 霉变大米清洗后食用 | ||
| C. | 利用地沟油制成食用油 | D. | 用亚硝酸钠腌制的肉制品 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
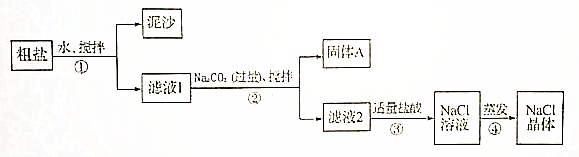
| A. | 滤液中一定有硝酸锌、硝酸铜、硝酸银 | |
| B. | 滤液中一定有硝酸锌、硝酸铜,可能有硝酸银 | |
| C. | 滤液中一定有银,没有铜和锌 | |
| D. | 滤液中一定有银和锌可能有铜 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题


| 温度t/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 |
| 溶解度S/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 |
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com