
【题目】木炭作为还原剂用于金属冶炼已有几千年历史。教材用如图Ⅰ所示实验介绍这一知识。

(知识回顾)
(1)木炭与氧化铜反应的化学方程式是_____,此反应中还原剂为_____。
(2)图Ⅰ中实验现象为_____。
A ①中黑色粉末变成红色
B ②中澄清的石灰水变浑浊
C ①中红色粉末变成黑色
D 生成二氧化碳气体
(3)图Ⅰ与教材中的装置还是略作了改进,实验结束时,可先用弹簣夹夹紧橡皮管,再熄灭酒精灯,这样做的目的除了防止石灰水倒吸入热的试管,避免试管炸裂外,还可以防止_____。
(拓展研究)
为了提高成功率,某研究小组设计如图Ⅱ方案进行实验。
分别称取2g木炭与CuO混合物,按每种比例重复实验3次,记录开始反应的时间及实验现象,实验记录如下表:
总质量相同(2g)但木炭与CuO比例不同的实验对比表 | |||||||
比例 | 1:6 | 1:7 | 1:8 | 1:9 | 1:10-1:11 | 1:12 | 1:13 |
加热时间 | 1′51″ | 1′43″ | 1′57″ | 2′21″ | 2′00″ | 1′53″ | 4′ |
实验现象 | 红热,产生大量气泡,石灰水变浑浊 | 偶尔红热,气泡较少 | |||||
实验结果 | 表层铜球较大,出现未完全反应的木炭粉末 | 反应较完全,生成网状铜块 | 部分生成Cu2O | 主要产物是Cu2O | |||
(4)装罩中酒精灯上的网罩作用是_____;
(5)由实验数据分析,除温度外,影响实验结果的因素是_____;
(6)从产物分析,该反应混合物的最佳比例范围是_____。
(装置改进)
(7)由于试管中有空气,实验时应注意:
①混合物需进行预热,除了使试管受热均匀外,另外的目的是_____。
②从理论上讲,并不能把石灰水变浑浊作为木炭跟CuO开始反应的充分证据。其理由是_____(用方程式表示)。
【答案】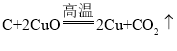 碳 AB 铜被重新氧化 使火焰更集中并提高温度 反应物的比例 1:10~1:11 减少试管内剩余空气的量,降低氧气对实验的影响
碳 AB 铜被重新氧化 使火焰更集中并提高温度 反应物的比例 1:10~1:11 减少试管内剩余空气的量,降低氧气对实验的影响 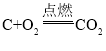
【解析】
(1)根据碳和氧化铜在高温的条件下生成铜和二氧化碳进行分析;
(2)根据碳还原氧化铜的实验现象分析;
(3)根据铜和氧气在加热的条件下生成氧化铜进行分析;
(4)根据加上灯罩可以使火焰更集中,提升温度进行分析;
(5)根据通过实验数据可以看出氧化铜和碳粉的比例不同,得到产物也不同;
(6)根据生成物分析,从实验结果中可以得出该题答案;
(7)①根据试管内有空气,空气中的氧气会消耗木炭进行分析;
②根据装置内有空气,在加热时遇到木炭会生成二氧化碳进行分析。
(1)碳和氧化铜在高温的条件下生成铜和二氧化碳,化学方程式为: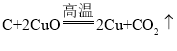 ,碳夺取氧化铜中的氧元素,生成二氧化碳,碳是还原剂;
,碳夺取氧化铜中的氧元素,生成二氧化碳,碳是还原剂;
(2)碳和氧化铜在高温的条件下生成铜和二氧化碳,氧化铜是黑色粉末,铜的颜色是红色,反应生成的二氧化碳使澄清的石灰水变浑浊,故图Ⅰ中碳还原氧化铜的实验现象为:①中黑色粉末变成红色;②中澄清的石灰水变浑浊;D选项生成二氧化碳气体属于实验结论,故选项A和B 正确;
(3)铜和氧气在加热的条件下生成氧化铜,所以除了防止石灰水倒吸入热的试管,使试管炸裂外,还可以防止铜被重新氧化;
(4)加上灯罩可以使火焰更集中,提升温度,利于反应的进行;
(5)实验研究:通过实验可以看出氧化铜和碳粉的比例不同,得到产物也不同,由实验数据分析,影响实验的另一因素是:反应物的比例;
(6)从实验结果中可以得出:反应物的比例为1:10~1:11时,反应较完全,生成网状铜块,故该反应混合物的最佳比例范围即反应最充分的是:1:10~1:11;
(7)①由于试管内有空气,混合物需进行预热,除了使试管均匀受热外,目的是:减少试管内剩余空气的量,降低氧气对实验的影响;
②由于装置内有空气,在加热时遇到木炭会生成二氧化碳,所以不能把石灰水浑浊作为木炭跟CuO反应的充分证据,试管中还可能发生反应:碳和氧气反应也会生成二氧化碳,反应的化学方程式为: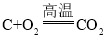 。
。


科目:初中化学 来源: 题型:
【题目】下列说法正确的是( )
A.同种元素在不同化合物中能出现不同的化合价,但在同一化合物中只有一种 化合价
B.过氧化氢是由氢元素和氧元素组成
C.当 SO2和 CO2的质量比为 1:1时,其氧原子个数比为16:11
D.元素金、铝、银、氯的元素符号中第一个字母书写相同
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁是最常见的金属,有广泛的用途.
(1)铁在潮湿的空气中最容易生锈,试用稀盐酸除锈的化学方程式是_____. 一般情况下,两种活动性不同的金属在潮湿环境中接触时,活动性强的金属首先 被腐蚀.造船工业为了避免乱串的钢铁外壳被腐蚀,通常在轮船外壳镶嵌的金属 是_____(填字母序号)
A 银 B 铜 C 铅 D 锌
(2)向硝酸银,硝酸铜,硝酸镁的混合溶液中加入一些铁粉,待完全反应后, 再过滤,下列情况说法正确的是_____.
A 滤纸上有 Ag,滤液中有 Ag+、Cu2+、Fe2+、Mg2+
B 滤纸上有 Ag、Cu,滤液中有 Ag+、Fe2+、Mg2+
C 滤纸上有 Ag、Cu、Fe,滤液中有 Fe2+、Mg2+
D 滤纸上有 Ag、Cu、Fe、Mg,滤液中有 Fe2+.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:

(1)25℃时,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为_____g.
(2)现有操作步骤:a溶解 b过滤 c降温结晶 d加热浓缩;若甲固体中含有少量乙,则提纯甲的操作步骤是_____(填字母序号).
(3)将35℃时丙的饱和溶液降温到25℃,则其溶液的溶质质量分数______填“变大”、“变小”或“不变”).
(4)向100g35℃的水中加入45g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出.你认为“全部溶解”的原因可能是_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学符号或相关化学知识填空:
(1)保持氢气化学性质的最小粒子_____;
(2)硝酸铵中氮元素化合价_____;
(3)地壳中含量最高的金属元素和含量最高非金属元素形成的化合物_____;
(4)能导致酸雨的氧化物(任写一种)_____;
(5)已知磷原子的相对原子质量为31,则磷原子的中子数为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
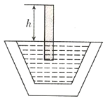
【题目】新鲜的冬瓜内盛有![]() 的氯化钠溶液,现将一木块放入此溶液中,木块处于漂浮状态,木块露出水面的部分高为
的氯化钠溶液,现将一木块放入此溶液中,木块处于漂浮状态,木块露出水面的部分高为![]() ,如图所示。问过一天后的
,如图所示。问过一天后的![]() 值与原来相比(不考虑水的蒸发现象)( )
值与原来相比(不考虑水的蒸发现象)( )
A.变大B.变小
C.不变D.不能确定
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请按要求完成下列物质性质的实验:
研究一:金属与酸反应过程中的能量变化。
(1)打磨后的镁条与稀盐酸反应,试管外壁发烫,说明该反应_____(填“放热”或“吸热”),反应的化学方程式为:_________;
(2)实验测得反应中产生气体的速率(v)与时间(t)的关系如下图,请根据t1~t2时间段反应速率变化,说明化学反应速率受__________等因素影响。

研究二:金属与氧气的反应:
(3)将一镁条取出发现其表面有一层灰白色物质,猜想这一物质可能是:______。(填化学式)
(4)再将镁条用砂纸打磨,表面变为光亮的银白色,用坩埚钳夹住镁条在酒精灯上点燃观察到的现象为:_____________。
(5)写出镁在空气中燃烧的化学方程式式:_________。由此说明,化学反应常常伴随能量的变化。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室制取气体所需装置如图所示。

(1)化学实验室常采用大理石和稀盐酸制取二氧化碳气体,该反应的化学方程式为____,所选用的发生装置是____。
(2)过氧化氢溶液长期保存会分解,使得溶质质量分数减小。小英从家中拿来一瓶久置的医用过氧化氢溶液和同学们一起测定该溶液的溶质质量分数。他们取出该溶液102g,加入适量二氧化锰生成O2的质量与反应时间的关系如图2。计算该过氧化氢溶液的溶质质量分数____。(请在答题纸上写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】对于化学反应,我们不但要考虑加入的试剂,还要考虑环境中的其他物质对化学反应的影响。教材中“木炭还原氧化铜”的实验(见下图),你认为试管A中的物质除木炭与氧化铜外,还存在_______________________。

(1)根据你所学化学知识猜测:试管A中除C、CuO外,还可能有物质___________(写化学式,下同)参与反应。除木炭还可以还原氧化铜外,经反应生成的_________也可以还原氧化铜。写出相应的化学方程式_________________________________。要排除环境对该反应的影响,你认为应采取何种措施?______________________________________________。
(2)请你推测,进入试管B的气体,除二氧化碳外,还可能有______________________。
要想使进入试管B中的二氧化碳全部被吸收,应采取什么措施?______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com