
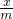 =
=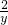
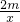
 =+2,所以其相对分子质量也可以变为:27×
=+2,所以其相对分子质量也可以变为:27× =18,所以质量相同的Al、Mg、Fe、Zn分别与足量的稀硫酸反应,产生氢气的质量依次减小.分析所给的选项可以知道选项D是正确的.
=18,所以质量相同的Al、Mg、Fe、Zn分别与足量的稀硫酸反应,产生氢气的质量依次减小.分析所给的选项可以知道选项D是正确的.

科目:初中化学 来源: 题型:
 (2005?白下区一模)某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的溶质质量分数相等的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如右图所示.下列对该图象理解的叙述中,正确的是( )
(2005?白下区一模)某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的溶质质量分数相等的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如右图所示.下列对该图象理解的叙述中,正确的是( )查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.Al>Mg>Zn>Fe | B.Al>Fe>Mg>Zn |
| C.Al>Zn>Fe>Mg | D.Al>Mg>Fe>Zn |
查看答案和解析>>
科目:初中化学 来源:《第8单元 金属和金属材料》2012年单元测试卷1(石龙中学)(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com