
【题目】化学实验室要从X、银、铜、锌四种金属混合物中分离某贵重金属.流程如下

其中错误的是
A.固体丙中一定只含银
B.四种金属活动性强弱顺序Zn、X、Cu、Ag
C.滤液C中只含有Cu(NO3)2
D.固体甲中一定含有Cu 和 Ag,可能含有X
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:初中化学 来源: 题型:
【题目】超细的铁微粒是一种纳米颗粒型材料,可在低温下将CO2分解为炭.下列推测不合理的( )
A. 超细铁微粒在反应中可能做催化剂
B. 该反应有助于减少温室气体排放
C. 该反应的另一产物可能是O2
D. 该反应属于化合反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关的化学用语表达正确的是
A. 五个氢原子:H5 B. 三个水分子:3H2O
C. 两个钙离子:2Ca+2 D. 四个铵根离子:4NH3+
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一烧杯中盛有42.2gCaCO3和CaCl2的粉末状混合物,向其中264.6g水,使混合物中的可溶物完全溶解。然后再向其中逐滴加如溶质的质量分数为10%的稀盐酸,烧杯中难溶固体物质的质量与所滴入稀盐酸的质量关系曲线如图所示。请根据题意回答下列问题:

⑴在滴入稀盐酸的过程中,观察到的明显现象是:
①_______________________
②_______________________
⑵当滴入10%的稀盐酸至图中A点时,烧杯中溶液里含有的溶质是(写化学式)______________。
⑶当滴入10%的稀盐酸146g时(即B点),试通过计算,求此时烧杯中所得不饱和溶液的溶质质量分数。______________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】空气是一种宝贵的自然资源.下列对空气的说法中正确的是
A.空气中含量最多的是氧气,氧气可支持燃烧
B.臭氧(O3)属于稀有气体,主要分布在距地面10~50km的高空
C.露天焚烧垃圾不会造成空气污染
D.随着工业的发展,排放到空气中的有害气体和烟尘对空气造成了污染
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】电视上广告用语没有科学性错误的是
A. 凡含有食品添加剂的实物对人体健康均有害,不可食用
B. 没有氧气就没有人类
C. 这种化妆品不含任何化学物质
D. 人长期在纯氧环境中,可以延年益寿
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】黄铁矿(主要成分为FeS2,杂质不含硫元素)是我国大多数硫酸厂制取硫酸的主要原料。化学课外活动小组为测定某黄铁矿中FeS2含量进行了如下的实验探究(假设每步反应均完全)。
【查阅资料】
①4FeS2+11O2 ![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
②Na2SO3+H2O2=Na2SO4+H2O
③Na2SO4+BaCl2=BaSO4 ↓+2NaCl
④Na2CO3+BaCl2=BaCO3 ↓+2NaCl
【实验探究】
Ⅰ. 称取1.60 g黄铁矿样品放入下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全。

Ⅱ. 反应结束后,将乙瓶中的溶液进行如下处理:

【问题讨论】
(1)Ⅰ中装置中甲瓶内盛放的试剂是氢氧化钠溶液,其作用是____________。
【含量测定】
(2)Ⅱ中最终得到的4.66g固体是_________(填物质的化学式)。
(3)计算该黄铁矿中FeS2的质量分数。_________(请写出计算过程)
【交流反思】
(4)如果缺少甲装置,则最终测得FeS2的质量分数将会_________(填“偏大”“偏小”或“不变”)。
(5)Ⅱ中证明所加BaCl2溶液过量的方法是_________________。
【拓展应用】
工业上以黄铁矿为原料生产硫酸的工艺流程图如下所示:

(6)接触室中发生反应的化学方程式为_________________。化学实验室现有质量分数为98%的浓硫酸,但在实验中常需要用到较稀的硫酸。要把100g上述浓硫酸稀释成质量分数为10%的硫酸,需要水的质量是________g,稀释时,应将_________沿烧杯内壁慢慢注入_______中,并不断用玻璃棒搅拌。硫酸是一种重要的化工产品,用途十分广泛,请写出稀硫酸的一种用途_______________。
(7)依据生产硫酸的工艺流程图,下列说法正确的是________(填字母)。
A.为使黄铁矿充分燃烧,需将其粉碎
B.催化剂能够提高SO2的反应速率和产量
C.SO2可做为生产硫酸的原料循环再利用
D.沸腾炉排出的矿渣可供炼铁
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】据2015年3月15日央视报道,北京市场九成的鸭血都是假鸭血,真正鸭血中含有人体所需的常见的金属元素,其中含有人体缺乏易导致贫血疾病的元素较高,该元素是( )
A. 钙 B. 锌 C. 铁 D. 碘
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸亚铁是一种重要的食品和饲料添加剂,某补血剂样品【主要成分为硫酸亚铁晶体(FeSO4xH2O)】,某化学兴趣小组对其产生了兴趣并进行了探究:
【探究一】硫酸亚铁晶体(FeSO4xH2O)热分解研究
【查阅资料】
1.无水硫酸铜粉末遇水会变成蓝色的硫酸铜晶体;
2.硫酸亚铁晶体加热时,先失去结晶水,高温会继续分解产生金属氧化物和气态非金属氧化物。
3.二氧化硫能使高锰酸钾溶液褪色。
【进行实验】该兴趣小组同学称取27.8g硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行分析,并利用SDTQ600热分析仪,对硫酸亚铁晶体热分解获得相关数据,绘制成图2所示的关系图,试回答:
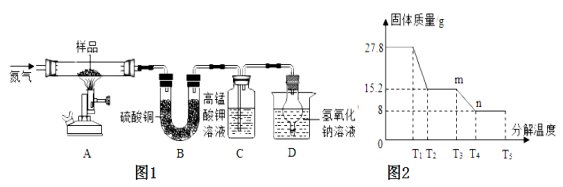
(1)装置B中硫酸铜粉末变蓝,说明产物中有 ,该物质的质量是 g;装置C中高锰酸钾溶液褪色,说明产物中还有 ;硫酸亚铁晶体完全分解后,装置A中的固体呈红棕色,放入足量稀盐酸,固体全部溶解,且得到黄色溶液,则该红棕色固体与稀盐酸反应的化学方程式为 。
(2)D装置中球形干燥管的作用是 。
(3)硫酸亚铁分解生成铁的氧化物和硫的两种氧化物,请写出化学反应方程式 。
(4)根据图2中的数据,请求出FeSO4xH2O中的x= 。(不写过程)
【交流讨论】实验中要持续通入氮气,否则测出的x会 (填“偏大”、“偏小”或“不变”)。
【探究二】补血剂样品中硫酸亚铁的含量:
①取10g补血剂样品研细后溶于40g水中,研细的目的是 ;
②向所配制的溶液中加氯化钡溶液至略过量,使其充分反应;
③过滤,洗涤,干燥,称量所得白色固体的质量为6.99g。
请计算出10g样品中FeSO4的质量分数,写出计算过程。此题2分。
(已知:FeSO4+BaCl2=BaSO4↓+FeCl2,有关相对分子质量:FeSO4—152,BaSO4—233)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com