(2013?沈阳一模)碳酸钠和碳酸氢钠是初中化学教材中出现的两种常见的盐,同时也是日常生活中有重要应用的物质,下面是阳阳小组进行的研究性学习过程,请你参与并回答相关问题.
【资料获悉】
(1)相同条件下,Na
2CO
3溶液比NaHCO
3溶液的碱性强;
(2)20℃时,Na
2CO
3、NaHCO
3的溶解度分别为21.3g和9.6g;
(3)NaHCO
3在270℃时能发生反应,而Na
2CO
3受热不易分解.
【探究过程】
实验一:阳阳同学想利用物理方法鉴别两种物质,请你参与或给予评价.
(1)可行,具体操作为
20℃时,各取10g两种样品,分别放入100g水中,充分溶解
20℃时,各取10g两种样品,分别放入100g水中,充分溶解
,实验现象及结论为
烧杯内固体能完全溶解的是Na2CO3,烧杯内固体不能完全溶解的是NaHCO3
烧杯内固体能完全溶解的是Na2CO3,烧杯内固体不能完全溶解的是NaHCO3
.
(2)不可行,理由是
若NaHCO3溶于水放热也会完全溶解
若NaHCO3溶于水放热也会完全溶解
.
★(提示:上述情况选择一种进行作答)
实验二:亮亮同学用酸碱度的差异鉴别Na
2CO
3和NaHCO
3.他应该选用
pH试纸
pH试纸
测定相同条件下两种溶液的PH,则pH较大的是
Na2CO3
Na2CO3
.
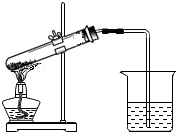
实验三:小明同学用加热的方法鉴别两种物质,具体操作为
分别取等量的两种固体放于试管内加热至270℃以上,并通入澄清石灰水
分别取等量的两种固体放于试管内加热至270℃以上,并通入澄清石灰水
,NaHCO
3发生分解反应的化学方程式为
.
实验四:小丽自己想出了一种新办法,取两种固体配制成溶液后,分别滴加过量澄清石灰水,结果都产生了白色沉淀,与小丽预想的只有碳酸钠溶液会产生白色沉淀的现象不符.小丽询问老师后得知,碳酸氢钠溶液也能与石灰水反应,请你将她的化学方程式补充完整:Ca(OH)
2+NaHCO
3═
CaCO3↓
CaCO3↓
+NaOH+H
2O.
【交流总结】通过本组同学的探究,作为组长的阳阳同学根据已有的知识及实验情况,总结出了鉴别碳酸钠和碳酸氢钠的方法主要有:
①通过溶解度差异来鉴别 ②用无色酚酞试液进行鉴别 ③用加热的方法进行鉴别④加入稀盐酸进行鉴别 ⑤加入澄清石灰水进行鉴别 ⑥通过酸碱度差异来鉴别
你认为其中可行的是
①③⑥
①③⑥
(填序号).
【拓展延伸】
1.小苏打在日常生活中用于生产食品,主要起发泡作用.通过上述研究性学习过程,你们认为小苏打(NaHCO
3)除用于食品工业外,在日常生活及实验室中还有哪些应用,试举一例:
治疗胃酸过多
治疗胃酸过多
.
2.在以后的学习中,我们还可以从定量的角度设计实验鉴别这两种盐.