
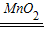 2H2O+O2↑;
2H2O+O2↑;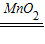 2H2O+O2↑;B;D;E;(3)将带火星的木条放在E装置瓶口处,若木条复燃,证明氧气已经集满;(4)量筒;(5)A;集气瓶中的液面上升;液体变红.
2H2O+O2↑;B;D;E;(3)将带火星的木条放在E装置瓶口处,若木条复燃,证明氧气已经集满;(4)量筒;(5)A;集气瓶中的液面上升;液体变红.

 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 2008年9月27日,太空第一次留下了“中国人的脚印”.我国研制的航天员舱外服为航天员成功进行太空行走提供了可靠的保证.
2008年9月27日,太空第一次留下了“中国人的脚印”.我国研制的航天员舱外服为航天员成功进行太空行走提供了可靠的保证.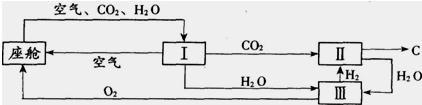
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
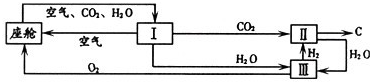
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com