
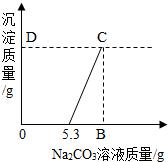
 有盐酸和氯化钙混合液100g,向混合液中加入Na2CO3溶液,生成的沉淀与加入的Na2CO3质量关系如图.若CaCl2在混合液中的质量分数为5.55%.
有盐酸和氯化钙混合液100g,向混合液中加入Na2CO3溶液,生成的沉淀与加入的Na2CO3质量关系如图.若CaCl2在混合液中的质量分数为5.55%.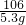 =
=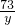
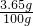 ×100%=3.65%
×100%=3.65%  =
=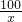 =
=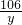


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:
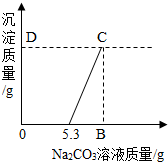 有盐酸和氯化钙混合液100g,向混合液中加入Na2CO3溶液,生成的沉淀与加入的Na2CO3质量关系如图.若CaCl2在混合液中的质量分数为5.55%.
有盐酸和氯化钙混合液100g,向混合液中加入Na2CO3溶液,生成的沉淀与加入的Na2CO3质量关系如图.若CaCl2在混合液中的质量分数为5.55%.查看答案和解析>>
科目:初中化学 来源: 题型:
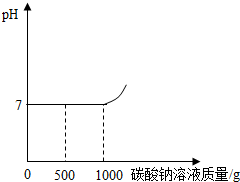
有盐酸和氯化钙的混合溶液l00g,向混合溶液中逐滴加入10%的![]() 溶液,生成沉淀的质量与加入
溶液,生成沉淀的质量与加入![]() 溶液的质量关系如图。若
溶液的质量关系如图。若![]() 在混合液中的质量分数为5.55%。求:
在混合液中的质量分数为5.55%。求:
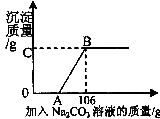
(1)在实验过程中,有沉淀生成,还可以看到的明显现象是___________
(2)C点的纵坐标所表示的质量。
(3)原混合液中HCl的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com