


科目:初中化学 来源: 题型:
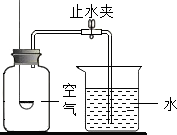 (2005?金华)将足量的下列物质分别放在燃烧匙上点燃(或灼烧),分别放入四只图示装置的广口瓶中,立即塞紧橡皮塞,反应结束待冷却后,打开止水夹,导管中水柱上升最少的是放入哪种物质的装置?( )
(2005?金华)将足量的下列物质分别放在燃烧匙上点燃(或灼烧),分别放入四只图示装置的广口瓶中,立即塞紧橡皮塞,反应结束待冷却后,打开止水夹,导管中水柱上升最少的是放入哪种物质的装置?( )查看答案和解析>>
科目:初中化学 来源:金华 题型:单选题
| A.铁粉 | B.磷 | C.木炭 | D.镁 |
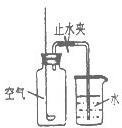
查看答案和解析>>
科目:初中化学 来源:2005年浙江省金华市中考化学试卷(解析版) 题型:选择题
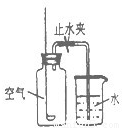
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com