
常见原子团的化合价
NO3__________,OH__________,SO4__________,CO3__________,NH4__________。
科目:初中化学 来源: 题型:
| 元素 | 11 Na 钠 |
12 Mg 镁 |
13 Al 铝 |
14 Si 硅 |
15 P 磷 |
16 S 硫 |
17 Cl 氯 |
18 Ar 氩 |
| 原子结构示意图 | 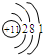 |
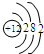 |
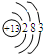 |
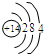 |
 |
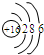 |
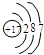 |
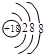 |
| (最高) 正化合价 |
+1 | +2 | +3 | +4 | +5 | +6 | +7 | -- |
| 负化合价 | -- | -- | -- | -4 | -3 | -2 | -1 | -- |
| 常见的几种离子 | H+ | Na+ | Ca2+ | OH- | Cl- | SO42- | CO32- | ||||||||||||||
| 元素和原子团的化合价 |
|
|
|
|
|
|
|
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 常见的几种离子 | H+ Na+ Mg+ O2- N
| ||||||||||||||
| 对应元素及原子团在化合物中的化合价 |
| ||||||||||||||
| 所能形成化合物的化学式 | Na2O,MgO,H2O | HNO3,H2CO3 | MgCO3,NaNO3 | ||||||||||||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 常见的几种离子 | H+、Na+、Mg2+ OH-、Cl-、SO42- | ||||||||||||||
| 对应元素及原子团在化合物中的化合价 |
| ||||||||||||||
| 所能形成化合物的化学式 | 酸 | 碱 | 盐 | ||||||||||||
| HCl、H2SO4 | NaOH、Mg(0H)2 | MgCl2、Na2SO4 | |||||||||||||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 常见的几种离子 | H+ Na+ Mg2+ OH- Cl- SO
| ||||||||||||||||
| 对应元素及原子团在 化合物中的化合价 |
| ||||||||||||||||
| 所能写出化合物的化学式 | HCl、 H2SO4 |
NaOH、 Mg(OH))2 |
MgCl2、 Na2SO4 | ||||||||||||||
| 写出相对应的名称 | 盐酸、 硫酸 |
氢氧化钠 氢氧化钠 、氢氧化镁 氢氧化镁 |
氯化镁 氯化镁 、硫酸钠 硫酸钠 | ||||||||||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com