
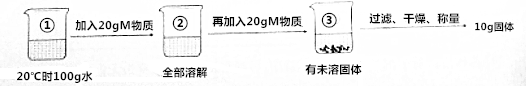

分析 (1)烧杯②中溶液的质量为溶质质量+溶剂质量;(2)根据在20℃时M物质的溶解度为该温度下,100g溶剂中最多溶解溶质的质量;(3)根据蒸发溶剂析出溶质质量考虑;(4)根据饱和溶液溶质质量分数计算方法考虑.
解答 解:(1)烧杯②中溶液的质量为溶质质量+溶剂质量=20g+100g=120g;
(2)根据在20℃时M物质的溶解度为该温度下,100g溶剂中最多溶解溶质的质量为:40g-10g=30g,所以溶解度是30g;
(3)根据第二次蒸发10g水析出晶体3g,所以第一次蒸发水,才析出晶体1g,所以烧杯①中的溶液为M的不饱和溶液;
(4)饱和溶液溶质质量分数计算,由于②③溶液都是饱和溶液,溶质质量分数相同.
故答案为:(1)120g;(2)30;(3)不饱和;(4)②③.
点评 解答本题关键是熟悉饱和溶液的定义,知道溶解度的四要素.


科目:初中化学 来源: 题型:解答题
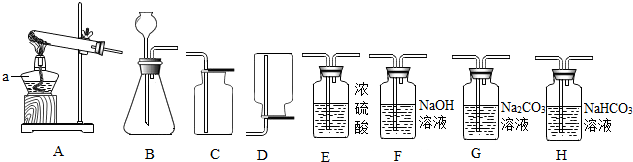
| 步骤和方法 | 现象 | 分析 |
| 取少量反应后的溶液,加入足量的CaCl2溶液 | 产生白色沉淀 | 发生反应的方程式: CaCl2+Na2CO3=CaCO3↓+2NaCl |
| 过滤,向滤液中加入少量NaOH溶液 | 产生白色沉淀 | 结论:猜想③正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 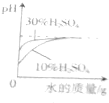 稀释等质量溶质质量分数分别为30%和10%的H2SO4溶液 | |
| B. | 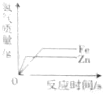 等质量的锌粉和铁粉,分别与质量分数相同的足量稀盐酸反应 | |
| C. |  在恒温条件下,将饱和的氯化钠溶液恒温蒸发水分至有白色晶体析出 | |
| D. | 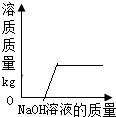 向氯化铜和硝酸铜的混合溶液中滴加氢氧化钠溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 青蒿素属于有机物 | |
| B. | 青蒿素的相对分子质量为282 | |
| C. | 一个青蒿素分子由15个碳原子、12个氢原子和5个水分子构成 | |
| D. | 青蒿素中碳、氢、氧三种元素的质量比为90:11:40 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 物质甲的化学式是CH4 | |
| B. | 该反应中分子和原子的种类都发生了改变 | |
| C. | 甲、乙两物质参加反应的质量比为1:2 | |
| D. | 图示反应属于复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
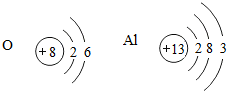 如图是氧和铝两种元素的原子结构示意图:
如图是氧和铝两种元素的原子结构示意图:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 属于氧化物 | |
| B. | 由碳原子、氢原子和氧原子构成的 | |
| C. | 相对分子质量为282g | |
| D. | C、H、O三种元素的质量比为90:11:40 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com