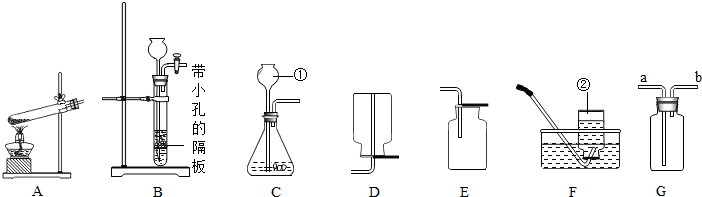
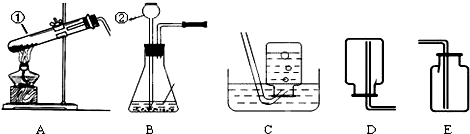
解:收集二氧化碳时导管要伸到集气瓶底部,收集满二氧化碳的集气瓶要正放在桌面上,如图:
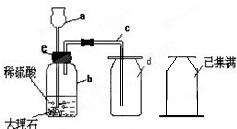
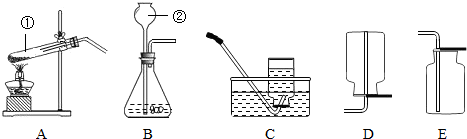
(1)这些是化学常见的仪器,结合其用途,a、长颈漏斗;b、广口瓶;c、导气管;d、集气瓶;e、双孔橡皮塞;
故答案为:长颈漏斗;广口瓶;导气管;集气瓶;双孔橡皮塞;
(2)实验室通常用稀盐酸与大理石(或石灰石)反应制取二氧化碳,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的方程式:CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑,故答案为:CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑;
(3)二氧化碳和水反应生成碳酸显酸性,能使紫色的石蕊试液变成红色,反应的方程式为:H
2O+CO
2=H
2CO
3;而碳酸不稳定,受热易分解为二氧化碳和水,酸性消失,故红色又变成紫色,反应的方程式为:H
2CO
3
H
2O+CO
2↑;故答案为:红色;H
2O+CO
2=H
2CO
3;紫;H
2CO
3
H
2O+CO
2↑.
分析:(1)熟练掌握常见化学仪器的名称及其用途;
(2)实验室通常用稀盐酸与大理石(或石灰石)反应制取二氧化碳,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,写出反应的方程式;
(3)根据二氧化碳和水反应生成碳酸及碳酸不稳定受热易分解分析.
点评:本题考查了实验室制取二氧化碳的原理以及二氧化碳的性质检验,要注意二氧化碳的特殊性质:溶于水且和水反应产生碳酸,显酸性,而二氧化碳本身不显酸性.

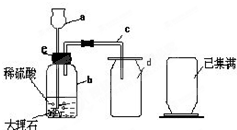 改正实验室制取二氧化碳中错误的操作(改在图上)
改正实验室制取二氧化碳中错误的操作(改在图上)
 H2O+CO2↑;故答案为:红色;H2O+CO2=H2CO3;紫;H2CO3
H2O+CO2↑;故答案为:红色;H2O+CO2=H2CO3;紫;H2CO3 H2O+CO2↑.
H2O+CO2↑.

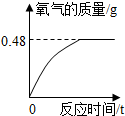 成氧气的质量与反应时间的关系如图所示:
成氧气的质量与反应时间的关系如图所示: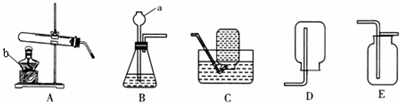
 如图是实验室用氯酸钾制氧气的装置图,请回答下列问题:
如图是实验室用氯酸钾制氧气的装置图,请回答下列问题: