
【题目】取敞口放置的氧化钙样品22g,加入足量盐酸,产生4.4g CO2,再向剩余溶液中足量的Na2CO3溶液,充分反应后,过滤得到沉淀质量为30g。下列说法正确的是( )
A. 样品固体中含有三种元素
B. 样品固体中碳元素的质量为1.6g
C. 样品固体中一定不含氢元素
D. 氧化钙在空气中发生的反应包含两种基本类型
科目:初中化学 来源: 题型:
【题目】A~H和X都是初中化学中常见物质,期中AD是无色气体,BE是红色固体,F为白色沉淀,H为红褐色沉淀,她们的转化关系如图所示
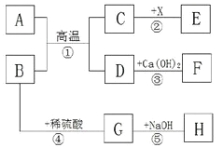
(1)写出化学式:A__ ___ ,H_ ,X__ ______
(2)写出反应③的方程式:
(3)写出反应④的方程式: ,该反应的反应类型是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列是电解水反应示意图和装置。示意图①~③中,“●”表示氢原子,“O”表示氧原子。
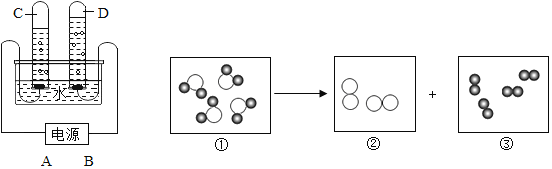
(1)图中表示化合物的是_____,表示单质的是_____(用序号填空)。
(2)②所代表的物质是左图中试管(填字母)_____中产生的气体,图中A是电源的_____(填“正”或“负”)极。
(3)为了探究C和D玻璃管分别产生的是什么气体,用燃着的木条分别在两个玻璃管口检验电解反应中产生的气体,观察并记录发生的现象,请填写下表:
C玻璃管 | D玻璃管 | |
现象 | _____ | _____ |
解释 | _____ | _____ |
(4)写出图中反应的化学符号表达式:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲图是一氧化碳还原氧化铁的装置,乙图是炼铁高炉示意图。下列叙述中正确的是
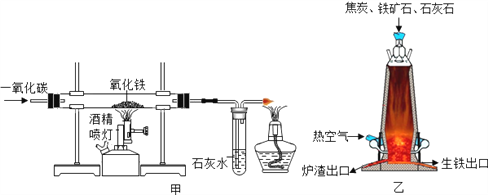
A. 炼铁的主要原理是:3CO+Fe2O3高温2Fe+3CO2
B. 乙图炼铁中原料焦炭的作用是只提供热量
C. 甲图中实验开始时应先点燃加热氧化铁的酒精喷灯
D. 两图中得到的铁是完全相同的
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,广口瓶中盛有气体X,胶头滴管中盛有液体Y,若挤压胶头滴管使液体滴入广口瓶中,振荡,一段时间后可见小气球a膨胀鼓起。下表中的各组物质不会出现上述现象的是( )
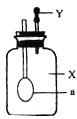
X | Y | |
A | CO | Ca(OH)2溶液 |
B | CO2 | NaOH溶液 |
C | HCl | Ca(OH)2溶液 |
D | SO2 | NaOH溶液 |
A. AB. BC. CD. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】东台将迎来高铁时代,高铁建设过程中使用到铝合金、钢铁等材料。
(1)列车制造需要的材料属于合成材料的是_____ (填字母序号)。
A 铜、铝、铁 B 涤纶 C 塑料 D 玻璃
(2)车身大量使用铝合金。铝的抗腐蚀性能较强,是因为_____。
(3)工业上用于高炉炼铁的原理是_____(用化学方程式表示);炼铁的固体原料需经过粉碎,其目的是_____。炉渣中含有硅酸钙( CaSiO3),其中硅元素的化合价是_____。
(4)为探究铜、铝、铁的金属活动性顺序,小明同学选用了下列药品进行实验,其中能验证铜、铝、铁的金属活动性顺序的是_____(填字母序号)。
A 铜丝、铁丝、氯化铝溶液
B 铝丝、铜丝、硫酸亚铁溶液
C 铝丝、铁丝、铜丝、稀盐酸
D 铁丝、氯化铝溶液、氯化铜溶液
(5)为了达到收旧利废节能减排的目的,从含有金属铝、铁、铜的粉末中,分离和提取出重要化工原料和有关金属,实验过程如下:
[查阅资料]
①2Al+2NaOH+2H2O=2NaAlO2+3H2↑( NaAlO2可溶于水)
(2)2NaA1O2+4H2SO4=Na2SO4+Al2(SO4)3+4H2O
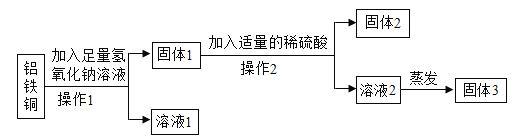
①操作1、2的都需要(填操作名称)_____、洗涤,若缺少洗涤,溶液2中将混有杂质 Al2(SO4)3和_____(填化学式):蒸发过程中要使用玻璃棒,其作用是_____。
②溶液1中溶质之一 NaAlO2属于_____(填“酸”“碱”“盐”或“氧化物”)。
第二步分离两种金属,除了加入稀硫酸外,还可选用下列试剂_____(填字母序号)。
A 硫酸铜溶液 B 硫酸亚铁溶液 C 稀盐酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组在实验室里进行木炭还原氧化铜的实验。
(实验1)装置如图。
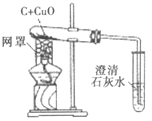
(1)木炭还原氧化铜的化学方程式为__,当碳与氧化铜的质量比为__(写最简整数比)时恰好完全反应。
(2)下列有关本实验的说法正确的是____(填字母)。
A 酒精灯加网罩以使火焰集中并提高温度
B 氧化铜发生了还原反应,木炭发生了氧化反应
C 观察到石灰水变浑浊即可证明氧化铜被还原了
D 反应后先撤出导气管,待试管冷却后再把其中的粉末倒出
(提出问题)实验1中,加热5分钟后仅能得到混有少量红色固体的黑色粉末。如何让木炭还原氧化铜时得到更多的铜呢?
(实验2)该小组同学在老师的指导下改进了实验,装置如图,加热2分钟后即得到紫红色有金属光泽的块状固体,且无黑色固体剩余。
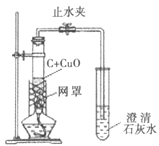
(1)刚烘干的木炭粉末与氧化铜粉末要在同一个研钵内充分研磨、混合均匀后再放入试管,这样做能使反应更充分,其主要原因是__。
(2)本实验所用的木炭与氧化铜的质量比为1︰10,碳需要略过量才能使氧化铜全部被还原,其主要原因是____。
(3)反应物放入试管后要尽量压实,并将试管竖直进行加热,使其下部完全被外焰包围,受热均匀,获得持续的高温。
(4)反应后关闭止水夹,让产物自然冷却,这时试管里残余的________就成了保护气。
(5)加了网罩的酒精灯火焰最高温度能达到800℃,而铜的熔点是1083℃。本实验获得了经熔化而成珠状或小块状的铜,可以推测木炭还原氧化铜的反应是________热量的。
(查阅资料)木炭还原氧化铜得到的铜中可能含有少量的氧化亚铜;氧化亚铜为红色固体,能与稀硫酸反应:Cu2O+H2SO4=CuSO4+Cu+H2O。
(拓展探究)将实验2得到的紫红色有金属光泽的块状固体全部研磨成粉末。
(1)将全部粉末放入烧杯中,加入足量稀硫酸,充分反应后,观察到______,证明实验2得到的铜中含有氧化亚铜;再经过滤、洗涤、干燥,得到纯净的单质铜1.52g。
(2)已知实验2使用的氧化铜粉末的质量为2.00g,不考虑实验过程中的损耗,则实验2得到的紫红色有金属光泽的块状固体中,单质铜的质量分数为______(计算结果保留一位小数)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线交于点P。据图回答:

(1)P点的含义是_____。
(2)t1℃时,30g的a物质加入到50g水中不断搅拌,能形成80g溶液吗?_____(填“能”或“不能”)
(3)t2℃时a、b、c三种物质的溶解度由大到小的顺序排列的是_____(填写物质序号)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】从公元1世纪起,铁便成了我国最主要的金属材料。

(1)工业上用CO与赤铁矿炼铁,反应的化学方程式为_______。
(2)“钢产量”是一个国家钢铁业结构性变化的标志。各国钢产量占世界比例如如图所示,从图中可获得的信息是__________(写出1条即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com