
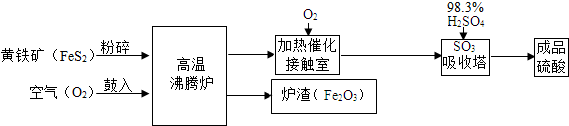
分析 (1)利用质量守恒定律分析;
(2)接触室内的反应是二氧化硫的催化氧化;
(3)根据题中的叙述找出反应物、生成物以及反应条件,然后依据质量守恒定律书写化学方程式;
(4)根据浓硫酸的稀释方法考虑;
(5)接触室内的反应是二氧化硫的催化氧化;
解答 解:(1)根据质量守恒定律,反应前后原子的种类和数目不变,反应前:Fe原子有4个,S原子有8个,O原子有22个,反应后Fe原子有4个,O原子有6个,所以空格部分为8SO2
(2)沸腾炉中生成的二氧化硫气体和空气中的氧气在接触室内发生的催化氧化反应生成三氧化硫;2SO2+O2$\frac{\underline{\;催化剂\;}}{△}$2SO3
(3)在高温的条件下,一氧化碳将氧化铁还原为铁,同时生成二氧化碳,故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(4)浓硫酸的稀释方法是:将浓硫酸沿着容器壁慢慢倒入水中,并用玻璃棒不断搅拌;
(5)a、粉碎矿石增大接触面积提高反应速率;
b、FeS2名称为二硫化亚铁中铁元素是+2价,设硫元素的化合价为x,+2+2x=0,x=-1,硫元素为-1价,二氧化硫中,硫显示+4价,三氧化硫中硫元素显示+6价,故错误;
c、催化剂改变速率,提高SO3 的产率,故正确;
d、二氧化硫和水会生成亚硫酸,三氧化硫和水会生成硫酸,可能会引发酸雨,故正确;
故为:acd;
故答案为:(1)8SO2;(2)2SO2+O2$\frac{\underline{\;催化剂\;}}{△}$2SO3;(3)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe;
(4)沿烧杯壁将浓硫酸慢慢倒入水中,并不断搅拌;(5)acd.
点评 解答本题的关键是要知道化学变化中的元素质量守恒特点,知道反应物接触面积越大,反应越剧烈,熟悉方程式的书写注意事项,知道浓硫酸的稀释方法.


科目:初中化学 来源: 题型:填空题
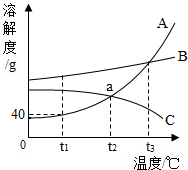 如图为A、B、C三种物质的溶解度曲线,据图回答:
如图为A、B、C三种物质的溶解度曲线,据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氯化钠可以配制生理盐水 | B. | 干冰可以用于人工降雨 | ||
| C. | 稀硫酸可以除铁锈 | D. | 氢氧化钠可以作食品干燥剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 管道通(如图)是一种常用的家用化工产品,能疏通毛发等造成的管道堵塞.小芳对家里买来的管道通产生了兴趣.小组的同学对管道通产生兴趣.
管道通(如图)是一种常用的家用化工产品,能疏通毛发等造成的管道堵塞.小芳对家里买来的管道通产生了兴趣.小组的同学对管道通产生兴趣.| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量管道通颗粒放入烧杯中,加入一定量水,搅拌 | 管道通溶解,有大量水蒸气 | 管道通溶解放热 |
| (2)取1所得溶液少量于试管中,滴加无色酚酞 | 酚酞试液变红色 | 溶液显碱性 |
| (3)取1所得溶液于试管中,加入少量铝粉 | 有气泡冒出 | 管道通能与铝反应 |
| 实验操作 | 实验现象 | 实验结论 |
(1)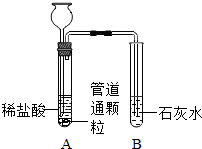 | 有气泡冒出,澄清石灰水变浑浊 | 该管道通中含有碳酸钠 |
| (2)取少量管道通配成溶液,滴加足量氯化钙溶液,再滴加无色酚酞溶液 | 酚酞试液变红色 | 该管道通中含有NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
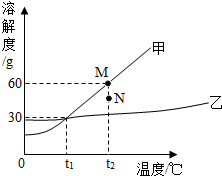
| A. | 甲的溶解度受温度影响比乙大 | |
| B. | t1℃时,甲、乙两物质饱和溶液中溶质的质量分数相同 | |
| C. | t2℃时,N点的甲溶液为饱和溶液 | |
| D. | 宜采用蒸发溶剂的方法得到乙晶体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 我国古代的“湿法炼铜”:2Fe+3CuSO4═3Cu+Fe2(SO4)3 置换反应 | |
| B. | 实验室用过氧化氢制取氧气:2H2O2$\frac{\underline{\;\;△\;\;}}{\;}$2H2O+O2↑ 分解反应 | |
| C. | 用氢氧化钠溶液吸收二氧化硫:2NaOH+SO2═Na2SO3+H2O 复分解反应 | |
| D. | 新制的生石灰加水能“煮熟”鸡蛋:CaO+H2O═Ca(OH)2 化合反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用氯化钡溶液区分稀盐酸和稀硫酸 | |
| B. | 用灼烧法区分棉纱线和羊绒线 | |
| C. | 用熟石灰区分尿素和氯化铵 | |
| D. | 用带火星的木条区分二氧化碳和氮气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com