
如图所示,为钠、镁、铝三种常见金属的原子结构示意图,

小明在资料中又找到下列粒子的结构示意图,请你分析以下的叙述中正确的是
| A.上述各原子中,最外层电子数都没有达到稳定结构 |
| B.核电荷数为18的粒子是失电子后形成的阴离子 |
| C.原子序数为19的金属元素的活动性,比原子序数为20的金属活动性强 |
| D.质子数为17、18的粒子都属于易得电子的非金属元素 |
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:初中化学 来源: 题型:阅读理解
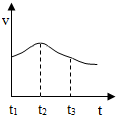 以下是甲、乙两同学对有关镁与盐酸反应的系列研究
以下是甲、乙两同学对有关镁与盐酸反应的系列研究查看答案和解析>>
科目:初中化学 来源: 题型:
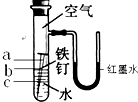 下表提供了在一定条件下,水能否与一些金属发生反应的信息.
下表提供了在一定条件下,水能否与一些金属发生反应的信息.| 物质 | 钠与冷水 | 镁与冷水 | 镁与水蒸汽 | 铁与冷水 | 铁与水蒸气 |
| 能否发生反应 | 剧烈反应 | 缓慢反应 | 不反应 | 加热条件下能反应 |
查看答案和解析>>
科目:初中化学 来源:2007年江苏省兴化市初三化学第一次模拟考试测试题上教版 题型:013
如图甲所示,为钠、镁、铝三种常见金属的原子结构示意图,小明在资料中又找到下列粒子的结构示意图(如图乙),请你分析以下的叙述中正确的是


A.上述各原子中,最外层电子数都没有达到稳定结构
B.核电荷数为18的粒子是失电子后形成的阴离子
C.原子序数为19的金属元素的活动性,比原子序数为20的金属活动性强
D.质子数为17、18的粒子都属于易得电子的非金属元素
查看答案和解析>>
科目:初中化学 来源:2012届江苏省兴化市初三第二学期第一次模拟考试化学试卷(解析版) 题型:选择题
如图所示,为钠、镁、铝三种常见金属的原子结构示意图,

小明在资料中又找到下列粒子的结构示意图,请你分析以下的叙述中正确的是

A.上述各原子中,最外层电子数都没有达到稳定结构
B.核电荷数为18的粒子是失电子后形成的阴离子
C.原子序数为19的金属元素的活动性,比原子序数为20的金属活动性强
D.质子数为17、18的粒子都属于易得电子的非金属元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com