





科目:初中化学 来源:不详 题型:填空题
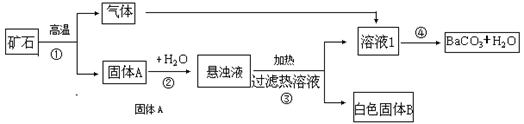
| 温度(℃) | 0 | 20 | 25 | 60 |
| Ba(OH)2溶解度 | 1.67 | 3.89 | 5.60 | 20.94 |
| Ca(OH)2溶解度 | 0.189 | 0.173 | 0.148 | 0.121 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | CaCl2溶液 | 稀盐酸 | 过量碳酸钙、过滤 |
| B | KOH溶液 | KCl | 适量稀盐酸 |
| C | NaCl溶液 | Na2CO3 | 适量硝酸钙溶液、过滤 |
| D | O2 | CO | 通过灼热的氧化铜 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
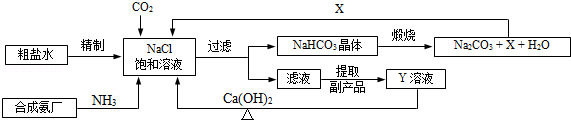
| 部分物质溶解性(室温) | |||
| | OH﹣ | SO42﹣ | CO32﹣ |
| Mg2+ | 不 | 溶 | 微 |
| Ca2+ | 微 | 微 | 不 |
| Ba2+ | 溶 | 不 | 不 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
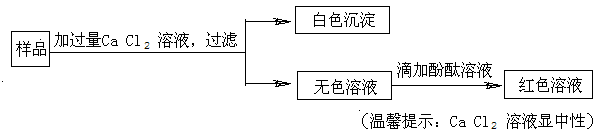
| A.CaCl2 | B.Na2CO3 | C.NaOH | D.Na2CO3和NaOH |
查看答案和解析>>
科目:初中化学 来源:不详 题型:推断题
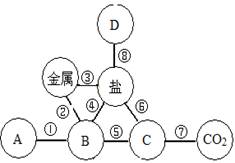
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.加入稀盐酸,有无色气体产生的物质中一定含有碳酸盐 |
| B.用燃着的木条伸入某气体中,火焰熄灭,则该气体一定是二氧化碳 |
| C.经点燃,产生蓝色火焰的气体不一定是一氧化碳 |
| D.尝一下,有咸味的白色固体一定是食盐 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
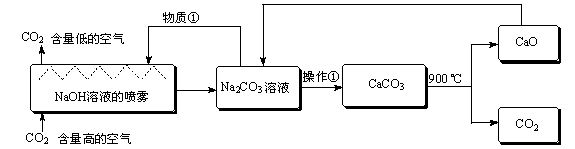
| A.该方法中包含复分解反应、分解反应、置换反应等 |
| B.物质①是NaOH溶液 |
| C.操作①是蒸发浓缩、降温结晶 |
| D.整个过程至少有2种物质可以循环利用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com