
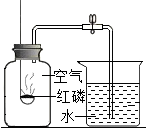
 如图装置常用来测定空气中氧气的含量.下列对该实验的认识中正确的是( )
如图装置常用来测定空气中氧气的含量.下列对该实验的认识中正确的是( )| A. | 使用红磷的量越多,最终进入集气瓶的水也越多 | |
| B. | 燃烧匙中的红磷可以换成细铁丝 | |
| C. | 该实验可说明N2难溶于水 | |
| D. | 若实验过程中,燃烧匙伸入集气瓶的速度太慢,会影响测定的结果 |
分析 A、根据空气中的氧气和红磷燃烧,减少的体积决定了进入水的体积进行分析;
B、根据所选物质要具备以下特征:(1)本身能够在空气中燃烧;(2)本身的状态为非气体;(3)生成的物质为非气态进行分析;
C、根据氮气的性质进行分析判断;
D、根据实验过程中,燃烧匙伸入集气瓶的速度太慢,会使集气瓶中的气体受热排出一部分进行分析.
解答 解:A、空气中的氧气和红磷燃烧,减少的体积决定了进入水的体积,氧气的体积决定了进入水的体积,故A错误;
B、细铁丝在空气中不能燃烧,不能用于测定空气中氧气的含量,故B错误;
C、该实验可说明氮气难溶于水,故C正确;
D、实验过程中,燃烧匙伸入集气瓶的速度太慢,会使集气瓶中的气体受热排出一部分,会影响测定的结果,故D正确.
故选:CD.
点评 本题难度不大,掌握测定原理(通过红磷燃烧消耗氧气,导致瓶内压强变小)、实验成功的关键(装置气密性要好;红磷要足量;要冷却到室温再读数)是正确解答此类题的关键.


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用10mL量筒量取6.8mL水 | |
| B. | 用托盘天平(精确度:0.1g)称取50g食盐 | |
| C. | 将100g10%的稀盐酸加热蒸发掉50g水,使得稀盐酸溶质质量分数变成20% | |
| D. | 用pH试纸测定某溶液的pH=5.6 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 实验设计 | 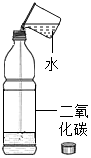 | 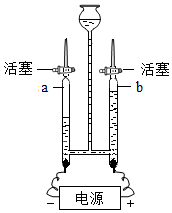 | 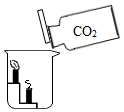 | 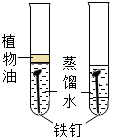 |
| 实验目的 | 证明二氧化碳与水反应生成碳酸 | 证明水是由氢元素和氧元素组成的 | 只能证明二氧化碳的密度比空气大 | 证明铁生锈是水和氧气共同作用的结果 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 鸡蛋壳的质量 | 空烧杯的质量 | 充分反应后,烧杯及内容物的总重量 |
| 16g | 60g | 155.6g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com