
分析 (1)根据金属的性质进行分析,金属的活动性越强,冶炼的程度越难,利用的越晚;
(2)根据在常温下铝与空气中氧气的反应来解答即可;
(3)根据铁生锈的条件分析;
(4)根据质量守恒定律进行分析.
解答 解:(1)金属的活动性越强,冶炼的程度越难,利用的越晚,所以,金属大规模开发和利用的先后顺序与金属的活动性有关;
(2)在常温下,铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步被氧化;所以,铝具有很好的抗腐蚀性能;
(3)铁在空气中锈蚀,实际上是铁跟氧气和水共同作用的结果;防止铁生锈的方法有刷漆、涂油地等;焊接铁制品时,通常先用稀盐酸除去其表面的铁锈;
(4)在②中左边铁、氯原子的个数分别是3、6个.由质量守恒定律可知:3X中共有铁、氯原子的个数分别是3、6个,则每个X中有1个铁原子.2个氯原子,X化学式是FeCl2.
故答为:(1)A;(2)铝与氧气反应,在其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步被氧化;(3)氧气,水,刷漆;(4)FeCl2.
点评 解答本题要求学生掌握常见金属的性质的知识并能熟练书写化学方程式,只有这样才能对相关方面的问题做出正确的判断.


科目:初中化学 来源: 题型:实验探究题
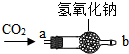 某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动.
某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动.| 实验操作 | 实验现象 | 实验结论 | |
| 猜想 | 在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水 | 有气泡产生,固体无剩余 | 猜想a、c不成立,猜想b成立. |
| 探究 | ①用带火星的木条伸入过氧化钠与水反应的试管中 | 木条复燃 | 生成物有氧气 |
| ②往①试管内的溶液中滴加无色酚酞试液(合理即可) | 酚酞试液变红(与操作对应) | 生成物有氢氧化钠 |
| 实验操作 | 实验现象 | 实验结论 |
| ①将CO2从a口处通入装置内,再把带火星的木条放在装置b口处 | 木条复燃 | CO2在常温下能与过氧化钠反应,该反应的化学方程式为: 2CO2+2Na2O2=2Na2CO3+O2 |
| ②取出充分反应后的固体生成物于试管中,往试管内滴加稀盐酸,将生成的氢气通入澄清石灰水中 | 有气泡产生 石灰水变浑浊 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
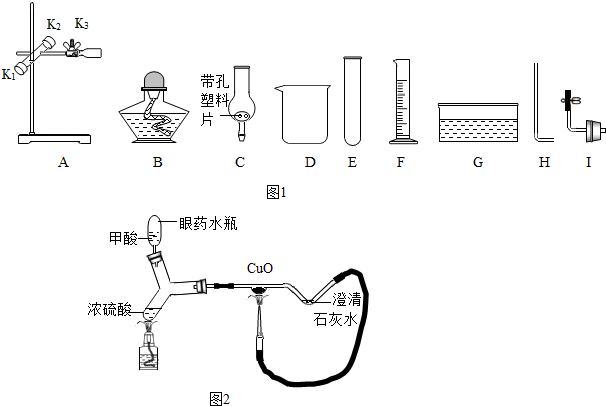
 我校“非常化学”兴趣小组同学在实验室拍下一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:
我校“非常化学”兴趣小组同学在实验室拍下一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小强和小华同学很感兴趣,决定对其成分进行探究:| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取少量该溶液于一洁净试管中滴加氯化钡溶液 | 产生白色沉淀 | 猜想②正确 相关的化学方程式BaCl2+Na2CO3═BaCO3↓+2NaCl. |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 质量/g | 170.00 | 166.00 | 164.00 | 163.00 | 162.40 | 162.08 | 162.08 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
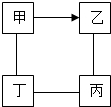 如图中“-”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可以直接转化为乙.下面四组选项中,符合如图要求的是( )
如图中“-”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可以直接转化为乙.下面四组选项中,符合如图要求的是( ) | 甲 | 乙 | 丙 | 丁 | |
| A | H2SO4 | NaOH | NaCl | Na2CO3 |
| B | CO | CO2 | H2SO4 | CuO |
| C | Fe | Fe2(SO4)3 | Mg | HCl |
| D | O2 | CO | CuO | C |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com