
【题目】下图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是
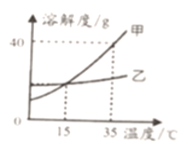
A. 15℃时,甲和乙的饱和溶液中溶质质量相等
B. 35℃时,30g甲加入50g水中,得到80g甲溶液
C. 从乙溶液中获得乙晶体,常用蒸发结晶的方法
D. 降低温度,甲溶液中溶质的质量分数一定减小
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】从大理石(主要杂质是氧化铁)中提纯碳酸钙的一种实验流程如下:
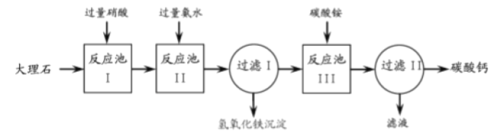
(1)反应池I中用硝酸不用稀硫酸的主要原因是______________。
(2)反应池II中加入氨水的目的是______________。
(3)反应池III用生成碳酸钙的化学方程式是______________。
(4)过滤II中所得滤液在农业生产中的一种用途是______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某复合肥的部分说明书如下图所示。请回答:

(1)从肥效的角度看,共有____种有效元素。
(2)该复合肥的有效成分之一是尿素[化学式为CO(NH2)2],则尿素中碳、氧、氮、氢的原子个数比为__。
(3)一袋该化肥至少含P2O5_________kg。
(4)从“注意事项”看,该复合肥料的物理性质是________,化学性质是_______(写一种)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为某钙片标签上的部分文字,请仔细阅读后回答下列问题。
(1)维生素D种类较多,其中维生素D2的化学式为C28H44O,试计算:
①维生素D2的相对分子质量________________;
②维生素D2中碳、氢、氧三种元素的质量比________________;
(2)计算每片钙片中含碳酸钙(CaCO3)的质量。_____________
(主要原料)碳酸钙、维生素D (功效成分)补钙 |
每片含钙(以Ca计)500 mg、维生素D100ug (食用方法)每日一次,每次一片 (规 格)2.5g/片 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请你根据所学知识并结合如图所示装置回答下列问题.
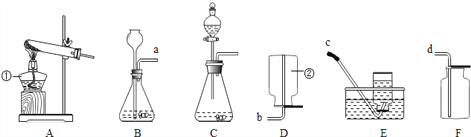
(1)写出图中标有①、②的仪器名称:①___________、②___________.
(2)用高锰酸钾制取氧气的化学方程式为______________________,发生装置应选___________,若收集氧气选择装置F,验满的方法是________________,集满氧气的集气瓶应___________(填“正”或“倒)放在桌面上,停止制气时应进行的操作是___________.
(3)晓华同学用大理石和稀盐酸反应制取二氧化碳气体,他应选择的发生装置是___,收集装置是____,反应的化学方程式是__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸钠广泛用于造纸、纺织、玻璃、洗涤剂、肥皂、制革等工业,是一种重要的化工原料。吕布兰、索尔维和侯德榜为碳酸钠的工业化生产作出了巨大贡献。
Ⅰ、吕布兰法
1789年,法国医生吕布兰(N.Leblanc,1742—1806)以食盐、浓硫酸,木炭和石灰石为原料,开创了规模化工业制取碳酸钠的先河,具体流程如下:

(1)碳酸钠俗称______。
(2)在高温条件下,②中发生两步反应,其中一步是Na2SO4和木炭生成Na2S和CO,该反应的化学方程式为______。
(3)③中“水浸”时通常需要搅拌,其目的是______。
(4)不断有科学家对吕布兰法进行改进,是因为此法有明显不足,请写出一条不足之处______。
Ⅱ、索尔维法
1892年,比利时工程师索尔维发明氨碱法制碳酸钠,又称索尔维法。原理如下:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl,2NaHCO3![]() Na2CO3+CO2↑+H2O。某兴趣小组采用下列装置模拟索尔维法制备碳酸氢钠,进而制得碳酸钠。
Na2CO3+CO2↑+H2O。某兴趣小组采用下列装置模拟索尔维法制备碳酸氢钠,进而制得碳酸钠。
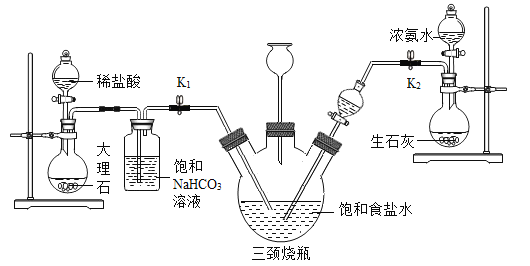
实验操作如下:
①关闭K1,打开K2通入NH3,调节气流速率,待其稳定后,打开K1通入CO2;
②待三颈烧瓶内出现较多固体时,关闭K2停止通NH3,一段时间后,关闭K1停止通CO2;
③将三颈烧瓶内的反应混合物过滤、洗涤、低温干燥,并将所得固体置于敞口容器中加热,记录剩余固体质量。
加热时间/min | t0 | t1 | t2 | t3 | t4 | t5 |
剩余固体质量/g | 未记录 | 15.3 | 13.7 | 11.9 | 10.6 | 10.6 |
请回答下列问题:
(5)饱和NaHCO3溶液的作用是除去CO2中混有的HCl,反应的化学方程式为______。
(6)三颈烧瓶上连接的长颈漏斗的主要作用是______,有同学认为应该在长颈漏斗内放置一团蘸有酸液的棉花,理由是______;关闭K2停止通NH3后,还要继续通一段时间
CO2,其目的是______。
(7)根据实验记录,计算t2时NaHCO3固体的分解率______(已分解的NaHCO3质量与加热前原NaHCO3质量的比值),请写出计算过程。若加热前NaHCO3固体中还存在少量NaCl,上述计算结果将_____(填“偏大”、“偏小”或“无影响”)。
(8)制碱技术在很长一段时间内把持在英、法等西方国家手中,我国化学工程专家侯德榜先生独立摸索出索尔维法并公布于众,又于1943年创造性地将制碱与制氨两种工艺联合起来,基本消除废弃物的排放,同时生产出碳酸钠和氯化铵两种产品,这就是著名的候氏制碱法。下列认识或理解正确的是______。
①科学认识是在曲折的、艰辛的积累过程中不断进步的;
②“科技兴邦、实业救国”是侯德榜先生回国研究的巨大动力;
③侯氏制碱法大大提高了原料的作用率,它符合当今“绿色化学”的理念。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一包白色粉末,可能由CuSO4、Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种组成,同学们查阅资料得知NaCl、CaCl2、BaCl2等溶液呈中性,经过思考,设计并进行了以下实验:
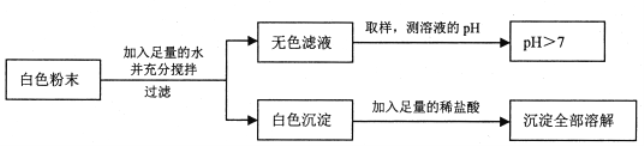
(1)白色粉末一定不含_____________,可能含有______________。
(2)为了确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究。
(提出问题)无色滤液中呈碱性的物质是什么?
(猜想假设)猜想一:NaOH
猜想二:______________
猜想三:Na2CO3和NaOH
(进行实验)
实验步骤 | 实验现象 | 结论 |
1.取少量该溶液于试管中 滴入_________溶液。 | _____________ | 猜想三正确 |
2.静置上述溶液,取少量上层清液于另一试管中,滴入几滴___________溶液。 | _______________ |
步骤1中发生反应的化学方程式为_______________。
(得出结论)白色粉末的成分是_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某环保小组监测到一造纸厂排放的废水中含有碳酸钠和硫酸钠两种物质,为测定废水中这两种物质的含量,环保小组的同学进行了以下实验:取该造纸厂排放的废水200g,先向其中加BaCl2溶液至ng后停止,然后再滴加稀盐酸,反应过程中加入溶液的质量与产生沉淀和气体的质量关系如图所示

(假设废水中其它成分不参与反应;钡的相对原子质量为137)
请根据图象与数据分析计算:
(1)a、b、c三点对应的溶液中所含BaCl2的质量关系是 (用“>”、“<”或“=”表示).
(2)m值等于 .
(3)该废水中硫酸钠的溶质质量分数(写出计算过程).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】英国科学家法拉第曾为少年儿童做过一个有趣的“母子火焰”实验,如图所示。回答下列有关问题。
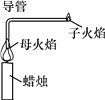
(1)子火焰的可燃物是________,蜡烛能产生母子火焰这一现象是由组成蜡烛的物质的重要物理性质决定的,该物理性质是______________________________。
(2)该实验成功的关键是导气管不宜太长,且导气管的起端必须插在蜡烛母火焰的中心部位,原因是:
①_______________________________________________;
②_______________________________________________。
(3)若蜡烛的主要成分是石蜡,则其燃烧的反应文字表达式为:_____________。
(4)某研究小组由法拉第的实验又联想到:在学习氧气的化学性质时发现:铁丝在氧气中燃烧没有火焰,而蜡烛在氧气中燃烧却有明亮的火焰。该小组同学进行了如下探究。
①写出铁丝在氧气中燃烧的文字表达式_______________________________________
②探究一:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如下图所示)。由此可知:蜡烛燃烧产生的火焰是由____________(填“固态”或“气态”)物质燃烧形成的。

③探究二:物质燃烧产生火焰的根本原因是什么? __________________________
(查阅资料)
物质 | 熔点╱℃ | 沸点╱℃ | 燃烧时温度╱℃ |
石蜡 | 50∽70 | 300∽550 | 约600 |
铁 | 1535 | 2750 | 约1800 |
钠 | 97.8 | 883 | 约1400 |
由上表可知:物质燃烧能否产生火焰与其____________(填“熔点”或“沸点”)和燃烧时温度有关。通过上表中石蜡、铁的数据对比,你认为物质燃烧时,什么情况下能产生火焰____________________________。由此推测:钠在燃烧时,________(填“有”或“没有”)火焰产生。
④ 根据硫在空气或氧气中燃烧的实验事实,请你推测硫沸点______硫燃烧时的温度(填“>”或“<”或“=”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com