��2012?���Ƹۣ�һ��ѧ��ȤС���ij�±���װ���еġ����������ܺ��棬���ǹ۲쵽�������������װ��ע�ijɷ�Ϊ���ۡ�����̿���Ȼ��ƣ����ֻҺ�ɫ�Ĺ����л���������������ɫ��ĩ��
�����ϻ�Ϥ����ϵ����������������ԭ�����������ܱ������������Ӷ��ﵽ�������ʵ�Ŀ�ģ�
����ʦָ�������������������ղ���Ϊ����ɫ��Fe
2O
3������������Բ��ƣ���
��̽��Ŀ�ġ�С��ͬѧ��̽���á����������Ƿ��Ѿ�ʧЧ�����������Ƿ��Ѿ���ȫ�������������ⶨ���ɷֵ��������������������̽��ʵ�飮
��ʵ��̽����
����1��С���ô����ӽ���Ʒ�����ִ��������˲��ֺ�ɫ���壮
����2����ȡ10.00g��Ʒ��һ�ձ��У�������ˮ��ֽ����ܽ���ˣ�������ϴ�ӡ�����Ƶ�������Ϊ7.28g��
����3��������װ�ã����õ���7.28g����������ϡ���ᷴӦ���õ��ӳӳƵ÷�Ӧǰ����������Ϊ0.15g��
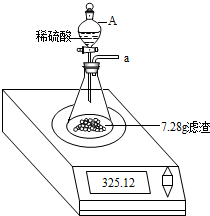
����4������ƿ�з�Ӧ���Һ����ˣ���������ϴ�ӡ�����Ƶ�������Ϊ1.20g��
���������ۡ�
��1���ɲ���1�ó��Ľ�����
��Ʒ�к��е��ʵ���
��Ʒ�к��е��ʵ���
��
��2������2Ŀ����
�ܽ���Ʒ���Ȼ���
�ܽ���Ʒ���Ȼ���
���������Һ�����ʵķ�����
ȡ������Һ���Թ��У��μ���������Һ��������ɫ������˵������Ϊ�Ȼ���
ȡ������Һ���Թ��У��μ���������Һ��������ɫ������˵������Ϊ�Ȼ���
��
��3������3������A������Ϊ
��Һ©��
��Һ©��
��
С����Ϊ0.15g��ֵ��ΪH
2�����������ɴ˼������Ʒ�е�����������Ϊ4.20g��
С�������װ�õ�a���ܴ�Ӧ��������һ��ʢ�м�ʯ�ҵĸ���ܣ�����������������
��ֹ�����ų�ʱ����һ����ˮ��ʹ�������������ӣ����ٶ����������IJⶨ���������
��ֹ�����ų�ʱ����һ����ˮ��ʹ�������������ӣ����ٶ����������IJⶨ���������
��
��4���������4������û�о���ϴ�ӣ���Ƶõ�����
��
��
1.20g���������=��������
����ʦָ������Ʒ��ϡ�����г���Fe��Fe
2O
3�ֱ�����ϡ���ᷴӦ�⣬�����ڷ�Ӧ��Fe+Fe
2��SO
4��
3=3FeSO
4����ˣ�С���ò���H
2������������Ʒ������������������ʵ���ϣ���Ʒ�е�����������Ӧ�������ᷴӦ���ĵ�������Fe
2��SO
4��
3��Ӧ�������������ܺͣ�
��ѧ��ʵ�顿С�콫����3��װ�ý����˸Ľ������³�ȡ10.00g��Ʒ����ʵ�飬��ȷ��ù���������ϡ���ᷴӦǰ����������Ϊ0.14g��
�����ݴ��������ڷ�Ӧ���̽ϸ��ӣ�С��ͬѧ����ʦ�İ����£��������Fe
2��SO
4��
3��Ӧ������������Ϊ0.56g��
��������롿
��1���Fe
2O
3��ϡ���ᷴӦ�Ļ�ѧ����ʽ��
��2��������������ݣ��������Ʒ�и��ɷֵ�����������




 �ִʾ��ƪϵ�д�
�ִʾ��ƪϵ�д�



