
【题目】下列各组物质按单质、氧化物、酸顺序排列的一组是( )
A.Fe;CO2;H3PO4
B.H2;H2O;NaOH
C.O2;NaOH;H2SO4
D.C;CaO;NaHSO4
 黄冈创优卷系列答案
黄冈创优卷系列答案科目:初中化学 来源: 题型:
【题目】聚合硫酸铁(PFS)是一种新型的饮用水处理剂和城市污水净化剂,其化学组成可表示为[Fex(OH)y(SO4)z]m . 某中学化学兴趣小组以聚合硫酸铁的生产流程和相关性质进行了一系列的探究. Ⅰ.聚合硫酸铁的工业生产.
如图是以回收废铁屑为原料制备PFS的一种工艺流程.
回答下列问题
(1)废铁屑主要为表面附有大量铁锈的铁,铁锈的主要成分为 . “过筛”与化学实验中的原理相似(填操作名称).
(2)酸浸时最合适的酸是 , 写出铁锈与该酸反应的化学反应方程式 .
(3)反应釜中加入氧化剂的作用是将Fe2+转化为Fe3+ . 你认为下列氧化剂中最合适的是(填标号),原因是 . A.KMnO4B.Cl2C.H2O2D.HNO3
(4)相对于常压蒸发,减压蒸发的优点是 .
A.有利于水分蒸发
B.降低沸点,防止晶体分解
C.降低生产成本
(5)Ⅱ.聚合硫酸铁的成分探究. 该研究小组为确定聚合硫酸铁的化学式,进行了如下实验:
①称取5.52g聚合硫酸铁样品溶于足量的稀盐酸中并充分混合;
②向①所得的混合物中加入足量的BaCl2溶液,充分反应后,经过滤、洗涤、干燥、称重,得沉淀4.66g.
③若向步骤②的滤液中加入过量的NaOH溶液,充分反应后,再将沉淀过滤、洗涤、灼烧、称重,得固体3.20g.
则聚合硫酸铁[Fex(OH)y(SO4)z]m样品中的x:y:z的值为 .
试写出该聚合硫酸铁与盐酸的反应方程式 .
(6)Ⅲ.聚合硫酸铁的热分解气体产物成分探究. 该小组将5.52g聚合硫酸铁在一定条件下加热完全分解,对所得气体产物进行实验探究.(已知SO3的熔点为16.8℃).
【提出假设】
假设1:所得气体的成分是SO3;
假设2:所得气体的成分是SO2、O2;
假设3:所得气体的成分是 .
(7)【设计实验】 按下图装置进行实验.
实验过程中发现:B中无水硫酸铜变蓝,C中U形管内有无色晶体析出,D中品红溶液褪色,装置E的作用是 .
【实验结论】
通过实验现象判断,假设成立.
如果最终试管中固体为一种红棕色纯净物,则质量为 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具,化学物质在日常生活中有重要用途.
(1)写出下列化学符号: ①两个氢原子; ②2个氨气分子;
③两个氢氧根离子; ④氧化钙中钙元素化合价;
⑤地壳中含量最多的元素 .
(2)选择适当的物质填空(填字母):A.氧气 B.干冰 C.熟石灰 D.小苏打 E.明矾 F.食盐
①改良酸性土壤;②急救病人;③腌制鱼肉等常用的调味品;
④人工降雨;⑤焙制糕点;⑥常用净水剂是 .
(3)写出化学方程式,并回答相关问题 ①铁丝在氧气中燃烧 .
②电解水 .
③盐酸除铁锈 .
④甲烷(CH4)完全燃烧 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来并加以利用.下图是利用氢氧化钠溶液“捕捉”CO2流程图(部分条件及物质未标出). 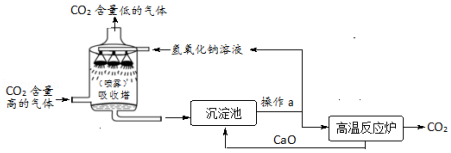
请根据有关信息回答问题:
(1)大量CO2直接排放到空气中会导致的加剧,破坏了人类生存的环境.
(2)用氢氧化钠溶液“捕捉”CO2的化学方程式是 , 氢氧化钠溶液喷成雾状的目的是 .
(3)操作a的名称是 , 该操作在实验室完成需要的玻璃仪器有烧杯、玻璃棒、 , 其玻璃棒的作用是 .
(4)上述流程中没有涉及到的基本反应类型是 .
(5)上述流程中,可以循环利用的主要物质有水、CaO、(填写化学式).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】物质的变化常常伴随在我们生活、生产中,下列变化属于化学变化的是( )
A.把木炭放入冰箱中,冰箱异味消失
B.夏天吃雪糕时,发现雪糕慢慢融化
C.用小刀削苹果皮后,一会儿表面呈黄色
D.工业上用分离液态空气制取氧气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业铁红的主要成分是Fe2O3 , 还含有少量的FeO、Fe3O4 . 为了测定铁红中铁的质量分数,兴趣小组的同学进行了如下实验,请你参与过程分析.
【资料1】草酸晶体(H2C2O43H2O)在浓H2SO4作用下受热分解,化学方程式为:
H2C2O43H2O ![]() CO2↑+CO↑+4H2O
CO2↑+CO↑+4H2O
(1)下列可用作草酸分解制取气体的装置是(填字母编号). 
(2)【问题讨论】用图所示装置进行实验: 
实验前应先 .
(3)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是、(填字母编号). a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(4)B装置的作用是 .
(5)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是: ①加热前 . ②停止加热后 .
(6)写出D装置中所发生反应的一个化学方程式 .
(7)【数据分析与计算】【资料2】铁的常见氧化物中铁的质量分数:
铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
铁的质量分数 | 77.8% | 70.0% | 72.4% |
称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数.
①D中充分反应后得到Fe粉的质量为m g,则<m< .
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是 .
【实验评价】
反思1:本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会(填“偏小”、“不变”或“偏大”).
反思2:请指出【问题讨论】中实验装置的一个明显缺陷 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】柠檬酸(C6H8O7)是一种较强的有机酸,在水溶液中可以解离出来H+ , 从而呈现酸性,主要用于香料或作为饮料的酸化剂.下列物质不能与柠檬酸反应的是( )
A.Mg
B.Fe2O3
C.CO2
D.NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com