
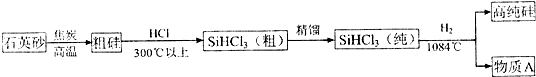


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
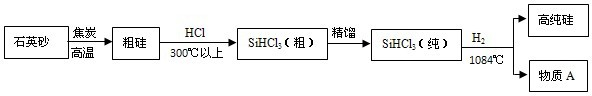
 从20世纪中叶开始,硅成了信息技术的关键材料,是目前应用最多的半导体材料.请回答下列问题:
从20世纪中叶开始,硅成了信息技术的关键材料,是目前应用最多的半导体材料.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
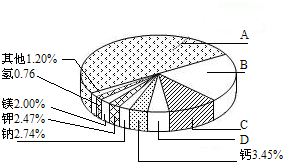
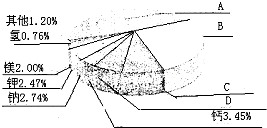
 ,从中不能获得的信息是
,从中不能获得的信息是| 1084℃ |
查看答案和解析>>
科目:初中化学 来源: 题型:
 从20世纪中叶开始,硅成了信息技术的关键材料,是目前应用最多的半导体材料.请回答下列问题:
从20世纪中叶开始,硅成了信息技术的关键材料,是目前应用最多的半导体材料.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com