
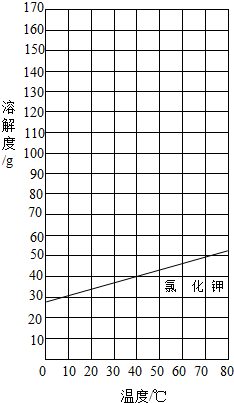
 (2013?江西)如表是氯化钾和硝酸钾在不同温度时的溶解度
(2013?江西)如表是氯化钾和硝酸钾在不同温度时的溶解度 | 温度/℃ | 0 | 20 | 40 | 60 | 80 | |
| 溶解度/g | KCI | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | |
 ;
;

 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:初中化学 来源: 题型:
 (2013?江西模拟)甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
(2013?江西模拟)甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:
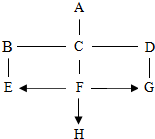 (2013?江西模拟)如图所示A~H是初中化学常见的物质.
(2013?江西模拟)如图所示A~H是初中化学常见的物质.查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
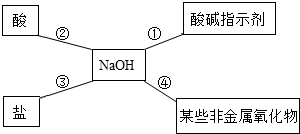 I.依据反应④说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为:
I.依据反应④说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为:| 实验操作 | 实验现象 | 实验结论 |
| 方案一:取少量样品溶于水,向其中滴入几滴的无色酚酞试液 | 溶液变红色 | 氢氧化钠没有变质 |
| 方案二;取少量的样品溶于水,置于试管中,向其中滴入足量的 BaCl2 BaCl2 溶液,再加入无色酚酞试液, |
溶液变浑浊,无色变红色 | 氢氧化钠部分变质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com