
【题目】庆祝中华人民共和国成立70周年的国庆阅兵让每一位中华儿女感到骄傲,空中飞行编队通过天安门广场时拉出的彩色烟雾一部分是由三氧化硫(分子结构图所示)遇到空气中的水形成的,下列关于三氧化硫的说法正确的是()

A.三氧化硫是有机高分子化合物
B.三氧化硫由硫、氧两种原子构成
C.三氧化硫中氧元素的质量分数最大
D.三氧化硫分子中硫、氧元素的个数比为1:3
科目:初中化学 来源: 题型:
【题目】在“宏观一微观”之间建立联系,是化学学科特有的思维方式。下图是某反应的微观示意图,下列有关该反应说法错误的是
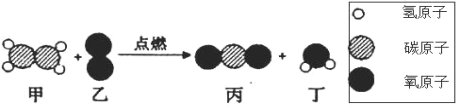
A. 反应前后原子个数不变B. 属于复分解反应
C. 生成的丙和丁的质量比为 22:9D. 反应前后分子个数不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】亚硫酸钠在印染、造纸等众多行业中有着广泛的应用。某研究小组采用如图实验流程用Na2CO3溶液吸收SO2制备Na2SO3。
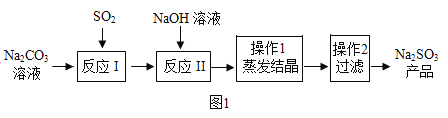
反应I中随着SO2的增加,依次发生如下化学反应:
SO+H2O+2Na2CO3=Na2SO3+2NaHCO3
SO2+2NaHCO3=Na2SO3+2CO2↑+H2O
SO2+H2O+Na2SO3=2NaHSO3
(1)H2SO3的名称为亚硫酸,则Na2SO3的名称为_____。
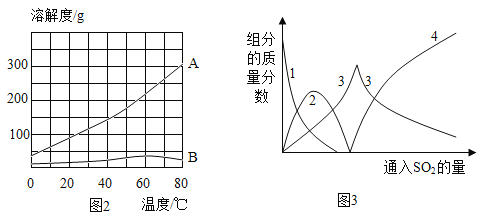
(2)常用蒸发结晶的方法分离混合溶液得到Na2SO3,由此可知,Na2SO3的溶解度曲线是与题图2中的_____(填A或B)物质的溶解度曲线相似。
(3)操作2得到的滤液中一定含有的溶质的化学式为_____。
(4)查阅资料可知,向碳酸钠溶液通入二氧化硫的过程中,溶液中有关组分的质量分数变化如图2所示。则线1表示_____(填化学式,下同)的质量分数的变化情况,线2表示_____的质量分数的变化情况。
(5)实验时,“反应Ⅱ”中加入NaOH溶液的目的是将反应1中生成的 NaHSO3转化为Na2SO3,则该化学反应方程式为_____。
(6)实验后,将Na2SO3样品放置在烧杯中,一段时间后,检测发现样品中出现Na2SO4杂质,且放置时间越长产生的Na2SO4越多,则Na2SO3样品变质为Na2SO4的化学反应方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用图1装置进行实验,先后将溶液快速全部推入,测得一段时间内压强变化如图2所示。下列说法不正确的是
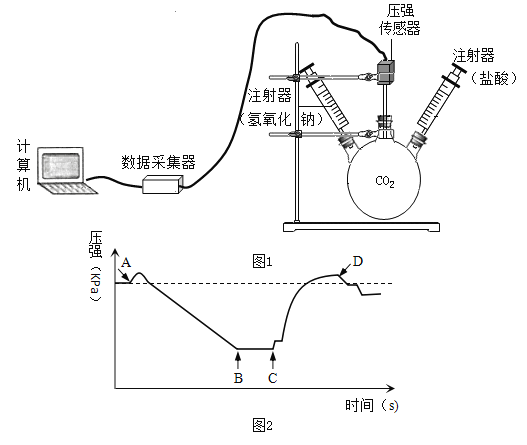
A.先推入的是NaOH溶液
B.BC段,CO2与NaOH反应基本停止
C.D点压强比初始瓶内压强大,此时瓶内二氧化碳气体的量比初始多
D.最终压强比初始压强小,可能是因为有部分二氧化碳溶于水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图所示的实验回答问题。
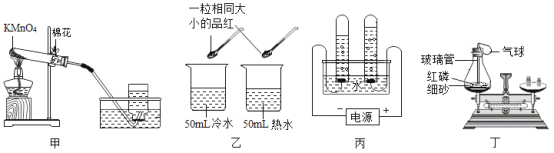
(1)甲中的化学方程式是______________。
(2)乙的目的是研究品红分子在水中的运动速率与_______________的关系。
(3)丙是电解水实验,反应的化学方程式为_______________;与电源正极相连的试管中产生的气体是______________。
(4)丁是验证质量守恒定律。其中红磷燃烧的化学方程式为____________;充分反应并冷却后,天平 仍保持平衡,从微观的角度解释其原因:_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分类、类比是初中化学常用的学习方法。初中化学有许多实验,若按照实验主要目的可将实验分为:物质发生化学反应条件的探究,物质性质的探究,物质含量的探究等。按实验目的将下列实验中的B与______(填字母)归为一类,分类的依据是______。
|
|
|
|
A | B | C | D |
(2)![]() 年,俄国学者贝开托夫
年,俄国学者贝开托夫![]() 在实验的基础上,根据金属和金属离子间互相置换的大小,以及金属跟酸、水等反应的剧烈程度,首先确定了金属活动性顺序,在这个顺序里包括了氢。在金属活动性顺序中活动性越强,其金属的还原性也越强。确定金属的活动性也可以根据元素在元素周期表中的位置判断,如图是元素周期表的一部分。请回答下列问题。
在实验的基础上,根据金属和金属离子间互相置换的大小,以及金属跟酸、水等反应的剧烈程度,首先确定了金属活动性顺序,在这个顺序里包括了氢。在金属活动性顺序中活动性越强,其金属的还原性也越强。确定金属的活动性也可以根据元素在元素周期表中的位置判断,如图是元素周期表的一部分。请回答下列问题。
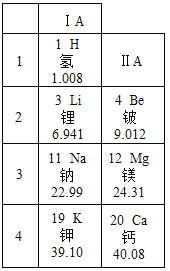
金属活动性顺序为:![]()
请推断金属铍的金属活动性比金属镁的活动性______(填“强”或“弱”);金属锂的还原性比金属镁的活动性______(填“强”或“弱”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,在乙瓶中放入用石蕊溶液染成紫色的干燥的纸花,在 A 处缓缓地持续通入混合气体 X,下表中的物质及实验操作后的现象对应关系不正确的是
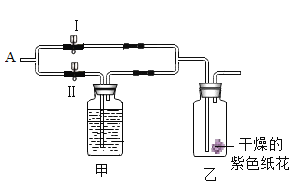
选项 | 气体 X | 甲中盛放的溶液(足量) | 关闭Ⅰ阀打开Ⅱ阀 |
A | 潮湿的混有一氧化碳的二氧化碳 | 浓硫酸 | 纸花不变色 |
B | 干燥的混有一氧化碳的二氧化碳 | 氢氧化钠溶液 | 纸花变为红色 |
C | 潮湿且混有氯化氢的二氧化碳 | 氢氧化钠溶液 | 纸花不变色 |
D | 干燥且混有氯化氢的二氧化碳 | 饱和碳酸氢钠溶液 | 纸花变为红色 |
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某学习小组同学欲利用绿色粉末碱式碳酸铜[Cu2(OH)2CO3]制备金属铜,并进行相关的实验。
[实验一]制备氧化铜并检验产物,装置如下图所示(省略夹持仪器)。
步骤一:打开弹簧夹,通入氮气。
步骤二:关闭弹簧夹,将A、B、C装置连接,并开始加热至A中固体质量不变,停止加热。
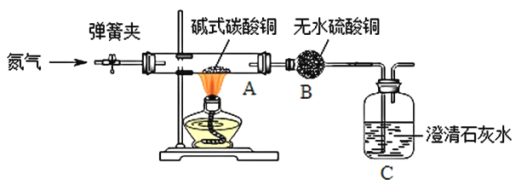
通入氮气的作用是________________;实验过程中,观察到A中有黑色固体生成,B中无水硫酸铜变蓝色、C中澄清石灰水变浑浊。碱式碳酸铜受热分解除了生成氧化铜,还生成了________________。装置C中反应的化学方程式为________________。
[实验二]用[实验一]中产生的氧化铜制备金属铜。
方法1:用一定量碳粉与[实验一] 中产生的氧化铜加热制取铜并检验产物。

实验过程中,观察到G中溶液变浑浊。E 中试管内固体反应的化学方程式是________________;装置F的作用是_____________________。
实验反思:为何[实验一]中步骤二需要加热至A中固体质量不变,才停止加热。分析可能的原因是____________________。
方法2:取适量[实验一]中产生的氧化铜,依据下列实验流程制取金属铜。

步骤I中反应的化学方程式是________________,观察到的现象是________________;步骤II中滤渣的成分是________________, 在滤渣中加入过量稀硫酸反应化学方程式是________________。
实验反思:在[实验二]中,你认为方法2优于方法1的理由是________________(写一条)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常会产生含硫酸的废水,需经处理至中性。某兴趣小组同学配制一定质量分数的氢氧化钾溶液来处理酸性废水。
(1)测定废水pH的方法是______。
(2)配制200 g质量分数为5.6%的氢氧化钾溶液
①计算:m(KOH)=___g,V(H2O)=______mL(水的密度近似为1.0gmL-1)
②称取氢氧化钾:调节托盘天平平衡后,将一只烧杯放在托盘天平的左盘,称量其质量.然后____(按操作先后顺序,填字母),直至天平平衡。
A 向烧杯中加氢氧化钾固体
B 按需要添加砝码、移动游码
③量取水: ④溶解; ⑤转移。
(3)定量测定废水:取酸性废水样品100g,逐滴加入5.6%的氢氧化钾溶液,废水中硫酸的质量分数变化如图所示。(假设废水中其他成分不与氢氧化钾反应)
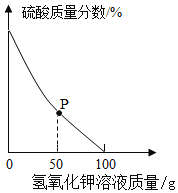
①P点对应溶液中一定存在的阳离子有_____(填离子符号)。
②废水中硫酸的质量分数为______(结果保留到0.1%).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com