考点:书写化学方程式、文字表达式、电离方程式,反应类型的判定
专题:化学用语和质量守恒定律
分析:书写化学方程式时,必须熟悉反应物、生成物和反应条件,必须遵守质量守恒定律,依据客观事实.只有熟悉四种基本反应类型的概念,才能作出正确的判断.
解答:解:(1)镁在点燃的条件下与氧气反应生成氧化镁,化学方程式为:2Mg+O
22MgO,其反应特征是“多变一”,属于化合反应;
(2)铁丝在点燃的条件下与氧气反应生成四氧化三铁,化学方程式为:3Fe+2O
2Fe
3O
4,其反应特征是“多变一”,属于化合反应;
(3)高锰酸钾在加热条件下反应生成锰酸钾、二氧化锰和氧气.该反应的化学方程式为:2KMnO
4K
2MnO
4+MnO
2+O
2↑,其特征是“一变多”,符合分解反应的概念,属于分解反应;
(4)双氧水在二氧化锰的催化作用下分解为氧气和水,该反应的方程式为:2H
2O
22H
2O+O
2↑,其反应特征是“一变多”,符合分解反应的概念;
(5)氢气与氧气在点燃的条件下反应生成水,该反应的化学方程式为:2H
2+O
22H
2O,其反应特征是“多变一”,属于化合反应.
故答案为:(1)2Mg+O
22MgO;化合反应;(2)3Fe+2O
2Fe
3O
4;化合反应;(3)2KMnO
4K
2MnO
4+MnO
2+O
2↑;分解反应;(4)2H
2O
22H
2O+O
2↑;分解反应;(5)2H
2+O
22H
2O;化合反应.
点评:本题主要考查化学方程式的书写和基本反应类型的判断,难度稍大.



 挑战100单元检测试卷系列答案
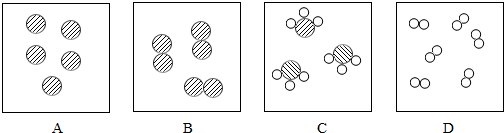
挑战100单元检测试卷系列答案 ”和“○”分别表示氮原子和氢原子.
”和“○”分别表示氮原子和氢原子.