
【题目】我国自主设计的大型客机成功试飞,国产航母下水,标志着我国的金属材料制造技术取得重大突破。根据所学知识回答下列问题:
金属 | A | B | C | D |
导电性(以100为标准) | 99 | 61 | 17 | 7.9 |
密度/(g﹒cm-3) | 8.92 | 2.70 | 7.86 | 11.3 |
熔点/°C | 1083 | 660 | 1535 | 327 |
硬度(以10为标准) | 3 | 2.7 | 5 | 1.5 |
(1)常温下一些金属的物理性质数据如表,据此可知高压输电线最好选用金属_____(填字母);C的合金通常可以做菜刀、锤子等,其合金的硬度_____5(填“>”“<”或“=”)。
(2)铁矿石有多种,如赤铁矿(主要成分Fe2O3)和磁铁矿(主要成分Fe3O4)等,写出磁铁矿的主要成分与一氧化碳反应的化学方程式_____。
(3)某兴趣小组为探究Zn、Fe、Cu、Ag四种金属的活动性,进行如下图中甲、乙、丙三个实验。
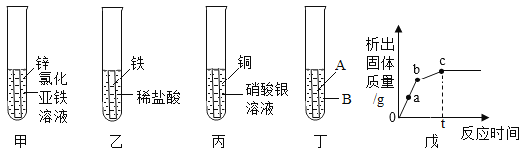
①小组同学随后发现该实验无法得出四种金属的活动性顺序。于是补充图丁实验,最终得出四种金属活动性:Zn>Fe>Cu>Ag,则图丁中的试剂A、B分别为_____(写出一组即可)。
③小组同学将丙试管中的物质过滤后、向滤液中加入甲中剩余的锌,析出固体质量的变化随反应时间的关系如戊图所示。写出a点对应溶液中所含的溶质是_____(填化学式)。
【答案】B >  铜、稀盐酸或铁、硫酸铜溶液(合理即可) AgNO3、Cu(NO3)2、Zn(NO3)2
铜、稀盐酸或铁、硫酸铜溶液(合理即可) AgNO3、Cu(NO3)2、Zn(NO3)2
【解析】
(1)高压输电线不仅要求要有较好的导电性,还要求密度小,所以选择金属B;由于合金的硬度大于纯金属的硬度,所以C的合金通常可以做菜刀、锤子等,其合金的硬度>5;
(2)在高温的条件下,四氧化三铁与一氧化碳反应生成铁和二氧化碳,化学方程式为: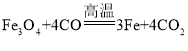 ;
;
(3)①甲乙丙实验已经得出:锌>铁,铁>H,铜>银,丁实验只要得出铁和铜的位置关系就可以,故可用金属和盐溶液,即铁和硫酸铜溶液或金属与酸反应,即铜、稀盐酸等;
②由于铁>铜>银,故锌加入后先置换银,固体质量增加,然后置换铜,固体质量增加比银要小,待硝酸铜反应完后,固体质量不再增加,a点对应锌与部分硝酸银反应,溶液中所含的溶质是剩余的硝酸银、硝酸铜和生成的硝酸锌。化学式分别为:AgNO3、Cu(NO3)2、Zn(NO3)2。


科目:初中化学 来源: 题型:
【题目】如图是由传感器采集实验相关信息描绘出的曲线,其中物质x表示能与二氧化碳反应的某液体,纵坐标y表示烧杯中的某个量。下列相关分析正确的是( )
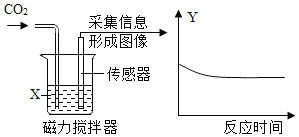
选项 | 物质X | 纵坐标y |
A | 水 | 溶液的质量 |
B | 水 | 溶液的PH |
C | 氢氧化钠溶液 | 溶质的质量 |
D | 氢氧化钙溶液 | 溶液中钙元素质量 |
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】同学们在实验室发现一瓶标签受损的无色溶液,如下图所示。教师希望同学们进行探究;确认这瓶溶液是什么溶液?
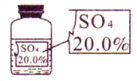
[提出猜想]
教师提示:实验室常用的含硫酸根离子的溶液有:
①硫酸镁溶液 ②硫酸钠溶液 ③硫酸溶液 ④硫酸铜溶液
小明同学首先提出猜想___________(填序号)不成立,原因是________________。
[查阅资料]
(1)常温下,相关物质的溶解度如下:
物质 | MgSO4 | Na2SO4 | CuSO4 | H2SO4 |
溶解度 | 35.1 g | 19.5g | 20.5g | 与水任意比互溶 |
(2) MgSO4、CuSO4的水溶液显酸性,Na2SO4的水溶液显中性
(3) Mg(OH)2、Cu(OH)2、BaSO4难溶于水
[实验探究]
为确定其成分,两个小组分别进行实验探究记录如下:
分组 | 实验操作 | 实验现象 | 实验结论 |
第一小组 | 取该溶液少许于试管中,向其中滴加几滴_____溶液 | 溶液中有白色沉淀生成 | 猜想①成立 |
第二小组 | 用玻璃棒蘸取少许原溶液滴在pH试纸上,并跟比色卡对照 | 溶液pH小于7 | 猜想③成立 |
[反思交流]
(1)结合实验及查阅资料,同学们讨论后认为猜想___________(填序号)不成立,原因是____________。
(2)其中一个小组存在不严密之处,分析原因是___________________,你有什么方法验证对应猜想?___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某学习小组的同学欲探究固体混合物A的组成,其中可能含有NaCl、NaOH、BaCO3、MgCl2四种物质中的两种或多种。实验过程和出现的现象如图所示:(设实验过程中所有发生的反应均恰好完全反应)
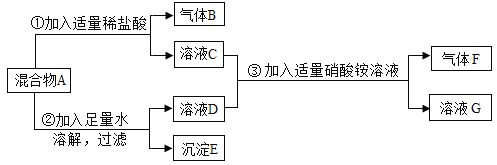
根据上述实验过程和发生的现象,请你回答下列问题:
(1)气体B的化学式为________。
(2)沉淀E____________(选填 “能”或“不能”)溶于稀硝酸。
(3)写出步骤①中生成气体B的化学方程式:______。
(4)固体混合物A中,肯定不存在的物质是________(写化学式)。
(5)在溶液C中,一定含有的酸根离子是________(写离子符号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)可用于净水,也可用作电池的电极材料,可通过下列反应制备:①MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O ②3Cl2+2Fe(OH)3+xKOH=2K2FeO4+6KCl+yH2O下列说法正确的是
MnCl2+Cl2↑+2H2O ②3Cl2+2Fe(OH)3+xKOH=2K2FeO4+6KCl+yH2O下列说法正确的是
A. 在反应①中,氯的化合价全部发生了改变
B. 反应②中x=10,y=6
C. 反应①②中共涉及了5种类型的化合物
D. 上述反应不属于四种基本反应类型中的任何一种
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学取氢氧化钠和碳酸钠的混合溶液50g装入烧杯中,每次滴加50g稀盐酸充分反应。测得部分数据及图像如下:
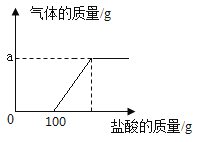
次数 | 1 | 2 | 3 | 4 | 5 |
加入稀盐酸的质量/g | 50 | 50 | 50 | 50 | 50 |
烧杯中物质的质量/g | 100 | 150 | 197.8 | 245.6 | 295.6 |
请根据有关信息计算:
(1)a的数值为________。
(2)稀盐酸中溶质的质量分数为_____。(写出计算过程)
(3)恰好完全反应后所得溶液中溶质的质量为_____。(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)可用于净水,也可用作电池的电极材料,可通过下列反应制备:①MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O ②3Cl2+2Fe(OH)3+xKOH=2K2FeO4+6KCl+yH2O下列说法正确的是
MnCl2+Cl2↑+2H2O ②3Cl2+2Fe(OH)3+xKOH=2K2FeO4+6KCl+yH2O下列说法正确的是
A. 在反应①中,氯的化合价全部发生了改变
B. 反应②中x=10,y=6
C. 反应①②中共涉及了5种类型的化合物
D. 上述反应不属于四种基本反应类型中的任何一种
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,鱼、肉的新鲜度不同,其浸出液pH会发生相应变化。鱼、肉的浸出液来判它们新鲜度,下列说法错误的是( )
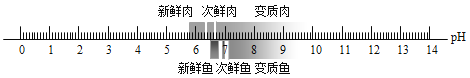
A.鱼肉的浸出液pH变大越趋向腐败变质
B.新鲜鱼肉漫出液比次鲜鱼肉的pH小,新鲜鱼肉浸出液比次鲜鱼肉酸性弱
C.新鲜鱼肉浸出液为酸性,能与活泼金属单质反应
D.变质鱼肉浸出液能使无色酚酞变红
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生产生活离不开化学
(1)可用____________方法来鉴别“人造羊毛”和“真羊毛”。
(2)冬天可用暖贴取暖。如图是常见“暖贴”的部分标签,暖贴中活性炭具有______作用。使用时空气进入暖贴,空气中的氧气与暖贴中的______发生反应使暖贴放热。

(3)粽子的原料一般有糯米、瘦肉、食盐、食用油等,其中富含糖类物质的是______________。
(4)钢筋混凝土可用来建造各种房屋,钢筋混凝土属于_____________材料。
(5)“共享单车”作为代步工具,既轻便灵活,又绿色环保。生产自行车需要消耗大量钢铁,工业炼铁的主要原理为_____________(用化学方程式表示)。为防止车架生锈,可采取的一种防锈措施是___________, 轮圈采用铝合金材料的优点是_______________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com