【答案】
分析:根据题目的叙述先分析出反应物、生成物、反应条件,以及质量守恒定律,再依此写出方程式.
解答:解:(1)反应物是木炭和氧气,生成物是二氧化碳,反应条件是点燃,所以方程式为:C+O
2
CO
2
(2)反应物是氢气和氧化铜,生成物是铜和水,反应条件是加热,所以方程式为:H
2+CuO
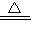
Cu+H
2O
(3)硫酸和硝酸钡发生复分解反应生成硫酸钡沉淀和硝酸,所以方程式为:H
2SO
4+Ba(NO
3)
2=BaSO
4↓+2HNO
3
(4)一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,故答案为:Fe
2O
3+3CO
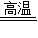
2Fe+3CO
2
(5)镁和二氧化碳在点燃的条件下生成氧化镁和碳,该反应由一种单质与一种化合物反应生成另一种单质和另一种化合物,符合置换反应的概念,属于置换反应,故答案为:2Mg+CO
2
2MgO+C;置换反应;
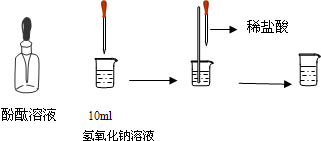
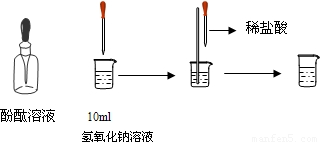
(6)则如图所示的化学反应中,过氧化氢分解生成水和氧气.该反应的化学方程式为:2H
2O
2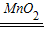
2H
2O+O
2↑
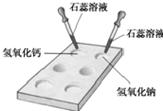
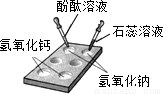
(7)反应特点为“一变多”,属于分解反应,反应的化学方程式:CaCO
3,
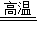
CaO+CO
2↑
反应特点为“多变一”,属于化合反应,反应的化学方程式:CaO+H
2O=Ca(OH)
2
反应特点为“二变二,两化”,属于复分解反应,反应的化学方程式:Ca(OH)
2+Na
2CO
3=2NaOH+CaCO
3↓
点评:在解方程式的书写题时,要首先知道反应原理,再分析出反应物、生成物以及反应条件,然后再写方程式.

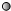 ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,则如图所示的化学反应方程式为: .
”表示氧原子,则如图所示的化学反应方程式为: .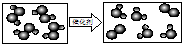
 CO2
CO2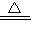 Cu+H2O
Cu+H2O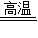 2Fe+3CO2
2Fe+3CO2 2MgO+C;置换反应;
2MgO+C;置换反应;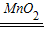 2H2O+O2↑
2H2O+O2↑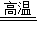 CaO+CO2↑
CaO+CO2↑

 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案