
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
(3)化合物中元素的质量=化合物的质量×化合物中该元素的质量分数.
解答 解:(1)次氯酸钙中钙、氯、氧三种元素的质量比40:(35.5×2):(16×2)=40:71:32.故填:40:71:32;
(2)次氯酸钙中氯元素的质量分数=$\frac{35.5×2}{40+(35.5+16)×2}$×100%≈49.7%.故填:49.7%.
(3)286g次氯酸钙中钙元素的质量=286g×$\frac{40}{40+(35.5+16)×2}×100%$=80g,故填:80.
点评 学生要能够根据物质的化学式看出相关的信息,如组成元素及原子个数等,能计算相对分子质量及元素的质量分数等.


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:初中化学 来源: 题型:解答题
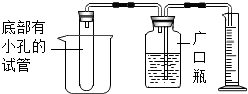 小科在学习了金属的化学性质后,想对锌、铜合金中锌的质量分数进行粗略测定.在老师的指导下,他设计了如图所示的实验装置,并选用了三种试剂:A.蒸馏水 B.锌、铜合金 C.稀硫酸.根据小科的实验思路,请你思考:
小科在学习了金属的化学性质后,想对锌、铜合金中锌的质量分数进行粗略测定.在老师的指导下,他设计了如图所示的实验装置,并选用了三种试剂:A.蒸馏水 B.锌、铜合金 C.稀硫酸.根据小科的实验思路,请你思考:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | a g氯酸钾与b g二氧化锰充分反应得到c g氧气,残留固体质量为d g,则d=a-c | |
| B. | 向饱和的硝酸钾溶液中加入5g硝酸钾固体,升高温度,硝酸钾固体质量增加 | |
| C. | 将100mL酒精与100mL水混合,能形成200mL溶液 | |
| D. | 向10g溶质质量分数为10%的NaCl溶液中加入10mL蒸馏水,溶液中溶质的质量是1g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
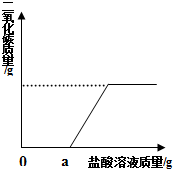 一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.| 样品质量 | 反应前总质量 | 反应后总质量 |
| 10.6克 | 148.5克 | 146.3克 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com