
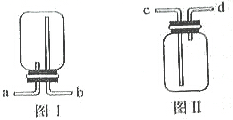
 如图是化学中“有名”的装置,有如下用途:
如图是化学中“有名”的装置,有如下用途:分析 (1)根据二氧化碳的密度以及排水法收集气体的方法来分析;
(2)氧气不易溶于水,如果通入水中会产生气泡;
(3)根据氧气不易溶于水,利用水的密度比气体大这一原理,可知应该从短管进入,把水从长管排出,若想知道收集的气体的体积,可以在排出水的导管连接一个量筒;
(4)干燥气体是长管进入气体,短管出气.
解答 解:(1)因为二氧化碳的密度比空气大,所以从a端进入,用排水法收集氧气,在集气瓶中装满水,氧气从b端进入;故填:a;b;
(2)氧气由于不易溶于水,所以在水中的氧气会以气泡的形式逸出.故答案为:d;产生气泡的速度;
(3)测定收集氧气的体积,则可先在集气瓶装满水,在c端放一个量筒,氧气从d端通入,通过进入量筒中水的体积即可测定收集氧气的体积.故填:c;量筒;d;量筒;
(4)干燥洗气是混合气体从长管进,纯净气体从短管出.故答案为:c.
点评 本装置是一个很重要的装置,具有多种功能,同学们一定要掌握它的具体使用方法.


科目:初中化学 来源: 题型:选择题
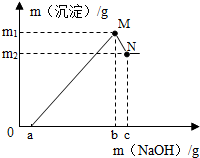 已知:MgSO4+2NaOH═Mg(OH)2↓+Na2SO4,Al2(SO4)3+6NaOH═2Al(OH)3↓+3Na2SO4,Al(OH)3+NaOH═NaAlO2+2H2O,Mg(OH)2不溶于NaOH溶液.现剪取wg镁铝合金的易拉罐壳,先用过量硫酸溶解,然后再向溶液中滴加NaOH溶液,反应符合如图关系(横坐标表示滴加NaOH溶液的质量,纵坐标表示生成沉淀的质量),则下列说法不正确的是( )
已知:MgSO4+2NaOH═Mg(OH)2↓+Na2SO4,Al2(SO4)3+6NaOH═2Al(OH)3↓+3Na2SO4,Al(OH)3+NaOH═NaAlO2+2H2O,Mg(OH)2不溶于NaOH溶液.现剪取wg镁铝合金的易拉罐壳,先用过量硫酸溶解,然后再向溶液中滴加NaOH溶液,反应符合如图关系(横坐标表示滴加NaOH溶液的质量,纵坐标表示生成沉淀的质量),则下列说法不正确的是( )| A. | a点表示NaOH溶液与剩余的硫酸恰好完全反应 | |
| B. | 在M点时,溶液中只有一种溶质 | |
| C. | N点表示Al(OH)3沉淀刚好完全溶于NaOH溶液 | |
| D. | 生成Mg(OH)2沉淀的质量为(m1+m2)g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
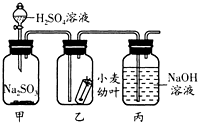 针对市场上一些不法商贩使用有毒的SO2气体对某些食品进行漂白,某科技兴趣小组以小麦幼叶为实验对象,研究SO2对植物的危害.他们通过查阅资料,得知硫酸溶液与固态的亚硫酸钠(Na2SO3)反应可产生硫酸钠和二氧化硫和水.设计实验如图所示.
针对市场上一些不法商贩使用有毒的SO2气体对某些食品进行漂白,某科技兴趣小组以小麦幼叶为实验对象,研究SO2对植物的危害.他们通过查阅资料,得知硫酸溶液与固态的亚硫酸钠(Na2SO3)反应可产生硫酸钠和二氧化硫和水.设计实验如图所示.| 室内 | 阳光下 | ||
| 出现烟斑时间 | 叶片变黄时间 | 出现烟斑时间 | 叶片变黄时间 |
| 30分钟 | 38分钟 | 15分钟 | 23分钟 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加热前,试管外壁有水,应该先擦干再加热 | |
| B. | 实验室用高锰酸钾加热制取氧气时,反应完毕后,应先撤去酒精灯,再从水槽中取出导气管 | |
| C. | 实验室制取氧气时,应先检查装置的气密性,再加入药品 | |
| D. | 对试管中的物体加热时,应先来回均匀受热再定点加热 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 小明学习了“蜡烛及其燃烧的探究”后,对蜡烛燃烧,酒精灯燃烧,家庭使用的液化气燃烧等产生了兴趣,于是开始了系列实验.
小明学习了“蜡烛及其燃烧的探究”后,对蜡烛燃烧,酒精灯燃烧,家庭使用的液化气燃烧等产生了兴趣,于是开始了系列实验.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
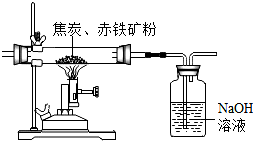 为了测定某赤铁矿中氧化铁的质量分数,化学兴趣小组的同学设计了两种实验方案(假设该赤铁矿中的杂质既不溶于水,也不发生反应).
为了测定某赤铁矿中氧化铁的质量分数,化学兴趣小组的同学设计了两种实验方案(假设该赤铁矿中的杂质既不溶于水,也不发生反应).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com