
【题目】柠檬酸(C6H8O7)是一种工业原料,广泛应用于食品、医药等行业。柠檬酸的水溶液显酸性,其一水柠檬酸(C6H8O7·H2O)的溶解度随温度升高变化较大。下图是用发酵液(主要成分是柠檬酸)制备一水柠檬酸晶体的工艺流程图。回答相关问题:
(1)气体X是(填化学式);
(2)加入硫酸,发生复分解反应的化学方程式为;
(3)操作1、2是 , 完成此操作时,需要的实验用品有铁架台、玻璃棒、烧杯、;
(4)操作3的目的是得到一水柠檬酸晶体,操作顺序是:蒸发浓缩、、过滤、洗涤、干燥;洗涤时,用冰水洗涤目的是;
(5)流程中的脱色时,可加入(填名称);
(6)母液可以循环利用,其中一定含有的溶质是。
【答案】
(1)CO2
(2)Ca3(C6H5O7)2+3H2SO4=3CaSO4 +2C6H8O7↓
(3)过滤,漏斗、滤纸
(4)降温结晶,降低溶解度,减小柠檬酸溶于水而带来损失
(5)活性炭
(6)柠檬酸
【解析】(1)碳酸钙和发酵液反应得到了柠檬酸钙和废液,依据质量守恒定律,所以发酵液中含有柠檬酸,柠檬酸显酸性,柠檬酸和碳酸钙反应会生成二氧化碳气体,所以气体X是:CO2;
(2)硫酸与柠檬酸钙反应生成硫酸钙沉淀和柠檬酸,其反应方程式为:3H2SO4+Ca3(C6H5O7)2═3CaSO4+2C6H8O7;
(3)经过操作1后得到了柠檬酸钙和废液,经过操作2后得到了滤渣硫酸钙和滤液,所以操作1、2的名称是:过滤;过滤使用的玻璃仪器有:漏斗、滤纸;
(4)通过柠檬酸的溶解度表可以看出,柠檬酸的溶解度受温度影响变化较大,所以要从柠檬酸的溶液中得到柠檬酸,需要先将柠檬酸蒸发浓缩制成高温时的饱和溶液,然后进行降温处理,可以得到柠檬酸晶体和母液,再进行过滤,可以得到柠檬酸晶体,故填 :降温结晶 降低溶解度,减小柠檬酸溶于水而带来损失;
(5)活性炭有吸附性,可以吸附色素和异味,明矾可以做絮凝剂,使水中的小颗粒沉降,肥皂水可以检验硬水和软水,所以工业生产中,可加入活性炭进行脱色处理;
(6)通过分析反应流程中的各种物质,可知得到柠檬酸晶体的母液,中含有一定的柠檬酸,可以在重新参与反应,所以母液可以循环,其中一定含有的溶质是:柠檬酸;
所以答案是:(1)CO2;(2)Ca3(C6H5O7)2+3H2SO4=3CaSO4+2 C6H8O7;(3)过滤,漏斗、滤纸;(4)降温结晶,降低溶解度,减小柠檬酸溶于水而带来损失;(5)活性炭;(6)柠檬酸.


科目:初中化学 来源: 题型:
【题目】请用所学的化学知识填空:
(1)氧气可用于抢救危重病人,是因为氧气能_____。
(2)古代用墨写的字保存很长时间不变色的原因是_____。
(3)分子和原子的本质区别是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列古诗文语句中不涉及化学变化或化学性质的是( )
A.日照香炉生紫烟,遥看瀑布挂前川
B.春蚕到死丝方尽,蜡炬成灰泪始干
C.落红本是无情物,化作春泥更护花
D.爆竹声中一岁除,春风送暖入屠苏
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】等质量的铁粉与过量的盐酸在不同的实验条件下进行反应,测定在相同时间t产生气体体积V的数据,根据数据绘制得到图1。
组别 | 盐酸的溶质质量分数 | 温度(℃) |
① | 7 | 30 |
② | 10 | 50 |
③ | 7 | 20 |
④ | 10 | 30 |
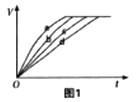
(1)请写出铁粉稀盐酸反应的化学方程式。
(2)由实验(填组别)可知,温度对于金属与酸反应速率的影响是。
(3)图1中表示第3组实验的曲线是。
(4)[进一步探究]图甲、图乙为利用数字化仪器测得的室温下足量的三种金属片分别与200ml100℅的稀盐酸反应产生氢气的量。(产生氢气的量由气体压强表示,在等温条件下,产生氢气体积与装置内压强成正比)。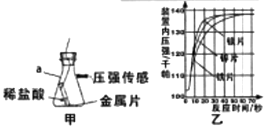
①实验中你认为,还要控制的变量是。
②由图乙,你得出的反应物的量与生成的气体体积的关系是。
(5)[拓展提高]下图为测得的室温下足量的镁片与20ml110℅的稀盐酸反应产生氢气的量与时间关系曲线,发现实验测得的实际值比通过计算得到的理论值偏大,请分析可能的原因(至少答两点)。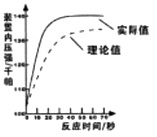
①。
②。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化石燃料的燃烧、硫酸的生产都产生二氧化硫,被雨水吸收后会形成酸雨,使农作物、建筑物等遭到破坏。工业烟气通常含有二氧化硫,在排放前需经脱硫处理.如图是两种常用脱硫工艺中含硫物质的转化路径(部分产物已略).请回答下列问题: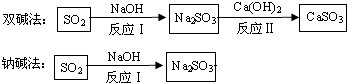
(1)CaSO3中Ca、S、O元素的质量比是 .
(2)已知原料NaOH的价格为5.8元/kg、Ca(OH)2的价格为0.74元/kg.两种工艺中,处理相同质量的SO2 , 所需的原料成本更低(填“双碱法”或“钠碱法”)。
(3)环保部门能较为精确测定某硫酸厂周围空气中二氧化硫的含量。取空气样品1000m3缓缓通过足量氯水(化学方程式:SO2+Cl2+2H2O=2HCl+H2SO4),在所得溶液中加入过量的氯化钡溶液,产生的白色沉淀质量为2.33g。试回答:
①通过测定雨水的来粗略判断其是否为酸雨。
②配制氯化钡溶液时,需用到的主要玻璃仪器有烧杯、量筒和。
③我国的环境空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示,请通过计算说明此空气中二氧化硫的浓度级别。
浓度限值(mg/m3) | ||
一级标准 | 二级标准 | 三级标准 |
0.15 | 0.50 | 0.70 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学反应中常伴随发生一些现象,这些现象可以帮助我们判断化学反应的发生.对下面实验现象的描述中,正确的是
A.木炭在空气中燃烧发出白光B.铜粉在空气中灼烧时,有黑色固体生成
C.酒精在氧气中燃烧时,生成水和二氧化碳D.纯净的氢气在空气中燃烧,产生黄色火焰
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“杨州八怪”之一清代著名画家郑板桥所作的字画至今仍不褪色,是因为墨汁中的碳( )
A.在常温下化学性质稳定B.具有还原性
C.具有可燃性D.具有氧化性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com