
【题目】化学是一门以实验为基础的自然科学。
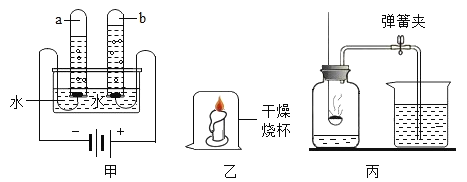
(1)用甲装置测定水的组成。负极与正极产生气体的质量比为_____。甲装置中发生反应的化学方程式为_____。
(2)小红同学用乙装置进行探究实验,观察现象得出结论:“蜡烛中含有氢元素”,该判断所依据的现象是_____。
(3)用丙装置测定空气中氧气的含量。下列有关该实验的说法中,错误的是_____(填字母)。
A 实验时红磷一定要足量 B 点燃红磷前先用弹簧夹夹紧乳胶管
C 红磷熄灭后立刻打开弹簧夹 D 最终进入瓶中水的体积约为消耗氧气的体积
(4)为测定金属氧化物着色剂中的金属含量,现将![]() 、
、![]() 、
、![]() 的混合物16克,与109.5克20%的稀盐酸混合后恰好完全反应,则此金属氧化物着色剂中金属元素的含量是_____。
的混合物16克,与109.5克20%的稀盐酸混合后恰好完全反应,则此金属氧化物着色剂中金属元素的含量是_____。
【答案】1:8 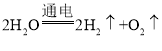 烧杯内壁上有水雾 C 70%
烧杯内壁上有水雾 C 70%
【解析】
(1)用甲装置测定水的组成。正极产生的气体是氧气,负极产生的气体是氢气。负极与正极产生气体的质量比为(1×2×2):(16×2)=1:8;水在通电的条件下分解,生成氢气和氧气,故甲装置中发生反应的化学方程式为: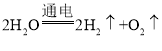 ;
;
(2)烧杯内壁上有水雾,证明蜡烛中含有氢元素;
(3)A、红磷要足量,将氧气完全消耗掉,选项正确;
B、为防止测量过程中水进入反应容器,一般点燃红磷前先用弹簧夹夹紧乳胶管,选项正确;
C、红磷熄灭后容器中温度较高,气体膨胀,为使结果更准确,一般是冷却到室温后再打开弹簧夹,选项错误;
D、红磷燃烧消耗氧气,冷却到室温后,装置内压强降低,在大气压的作用下,最终进入瓶中水的体积约为消耗氧气的体积,选项正确。故选C;
(4)氧化铁、氧化铜和氧化铝与稀硫酸反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O,CuO+2HCl═CuCl2+H2O:Al2O3+6HCl═2AlCl3+3H2O由于氧化铝、氧化铜和氧化铁的混合物与109.5克20%的稀盐酸混合后恰好完全反应,分析化学方程式可以知道氧化铝、氧化铜和氧化铁中的氧元素转变为水中的氧元素,即混合物中氧元素的质量和水中氧元素的质量相等,由方程式可得盐酸与水的关系式为2HCl~H2O,设生成水中氧元素的质量为x,109.5克20%的稀盐酸中氯化氢的质量=109.5g×20%=21.9g,则:
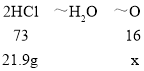
![]()
x=4.8g
则此金属氧化物着色剂中金属元素的含量=![]() ×100%=70%。
×100%=70%。


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:初中化学 来源: 题型:
【题目】鸡蛋壳的主要成分是碳酸钙,为了测定某鸡蛋壳中碳酸钙的含量,小群同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取10g放在烧杯里,然后往烧杯中加入足量的稀盐酸90g,充分反应后,称得烧杯中物质的总质量为97.8g。(假设鸡蛋壳中的其他物质不与盐酸反应)
(1)产生二氧化碳气体______g。
(2)10g该鸡蛋壳中最酸钙首质量是____g,要求写出完整的解题步骤。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】
N(NO2)3是科学家发现的一种新型火箭燃料,计算:
(1)N(NO2)3的相对分子质量_____
(2)N(NO2)3中氮元素和氧元素的质量比为_____
(3)N(NO2)3中氮元素质量分数为_____(结果保留一位小数)
(4)76gN(NO2)3所含氧元素多少克?_____(列式计算,结果保留一位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】通常状况下,乙烯(![]() )是一种无色气体,具有可燃性,其燃烧反应的化学方程式为:
)是一种无色气体,具有可燃性,其燃烧反应的化学方程式为:![]() ,则下列有关说法不正确的是( )
,则下列有关说法不正确的是( )
A.乙烯中碳元素的化合价为-2价
B.乙烯属于有机化合物
C.X中碳、氧元素的原子个数比为1︰2
D.该反应属于置换反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列关于乙醇(C2H5OH)说法正确的是( )
A.乙醇的相对分子质量是46g
B.乙醇是由碳原子、氢原子、氧原子组成
C.乙醇中碳、氧元素的质量比为3:2
D.等质量的乙醇和乙烯(C2H4)在氧气中完全燃烧时,耗氧量不相同
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】精还原铁粉是一种重要的化工原料,某兴趣小组对其进行下列研究:
(物质制备) 利用绿矾制备精还原铁粉的工艺流程如下:

粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式:
FexOy+yH2![]() xFe+yH2O、Fe3C+2H2
xFe+yH2O、Fe3C+2H2![]() 3Fe+CH4
3Fe+CH4
(1)写出焙烧中氧化铁与CO反应的化学方程式:__________________;
(2)焙烧中加入焦炭的作用:__________________、________________。(写出两条)
(含量测定)为得到精还原铁粉并测定粗还原铁粉中氧和碳元素的质量分数,按如下装置进行实验。
已知3CH4+4Fe2O3![]() 3CO2+6H2O+8Fe(假设每步反应都完全且不考虑装置内原有空气对测定结果的影响)。
3CO2+6H2O+8Fe(假设每步反应都完全且不考虑装置内原有空气对测定结果的影响)。
(3)主要实验步骤如下:
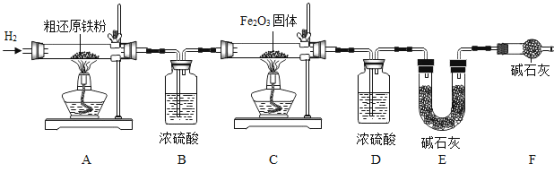
①按顺序组装仪器,检查装置的气密性,称量样品和必要装置的质量;②点燃A处酒精灯;③缓缓通入纯净干燥的H2;④点燃C处酒精灯;⑤分别熄灭A、C处酒精灯;⑥再缓缓通入少量H2; ⑦再次称量必要装置的质量。
操作的先后顺序是①→______→______→______→______→______→⑦。
步骤②和③能否交换?________(填“能”或“不能”),原因是_________________。
(4)步骤⑤和⑥能否交换?________(填“能”或“不能”),原因是_________________。
(5)装置F的作用是___________,若缺少装置F,则所测氧元素质量分数将______(选填“偏大”、“偏小”或“不变”下同),碳元素质量分数将_________。
(6)粗还原铁粉样品质量为5.0g,装置B、E分别增重0.54g和0.44g,则样品中氧元素质量分数为________;碳元素的质量分数为_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学对蜡烛(主要成分是石蜡)及其燃烧进行如下探究,请你填写下列空格。
(1)取一支蜡烛,用小刀切下一小块,把它入水中,蜡烛浮在水面。
结论:石蜡的密度比水______________。
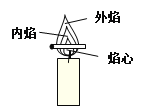
(2)点燃蜡烛,观察到蜡烛的火焰分为外焰、内焰和焰心三层。把一根火柴梗放在蜡烛的火焰中(如图)约1s后取出,可以看到火柴梗的____________处最先碳化。(变黑)。
结论:蜡烛火焰的___________层温度最高。
(3)再将一只干燥的烧杯罩在蜡烛火焰上方,烧杯内壁出现水雾。取下烧杯,迅速向烧杯内倒入少量澄清石灰水,振荡。澄清的石灰水变浑浊。
结论:石蜡烧燃后的生成物有________和________。
查看答案和解析>>
科目:初中化学 来源: 题型:
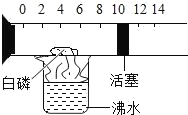
【题目】如图是一个具有刻度和活塞可滑动的玻璃容器,其中有空气和足量的白磷, 将它放在盛有沸水的烧杯上方,进行实验。请完成实验报告:
(1)实验目的:测定空气中____的体积分数。
(2)实验现象:白磷着火燃烧,活塞先右移,后左移,最后停在刻度约为_____(填整数)的位置上。
(3)实验结论:空气的成分按体积计算,____约占![]() 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com