
����Ŀ����ѧ�����Ի�ѧѧϰ�����°빦�������ã�
��1������������о���ѧ���ʵ���Ҫ��������ͼ1��ijͬѧ�����������仯�����֪ʶ����ͼ�� 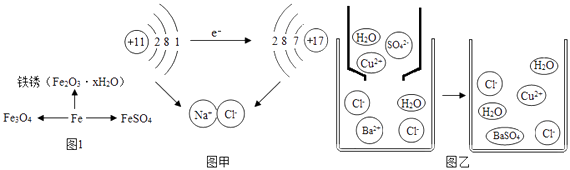
����˿ȼ������Fe3O4�Ĺ�������ѡ��ų��������ա���������
������Ʒ����ʴ���̣�ʵ��������������е��ȷ�����ѧ��Ӧ�Ĺ��̣�
����FeSO4����Ԫ�ػ��ϼ���ͬ����������Ļ�ѧʽ�� ��
��2��������ģ�ͻ����о���ѧ�仯����Ҫ������ ��ͼ��������������Ӧ�����Ȼ��Ƶ�ʾ��ͼ����ͼ˵���ڻ�ѧ��Ӧ������һ�������仯���� �� ������ĸ��
a��ԭ�Ӻ� b��ԭ�Ӻ����������� c��ԭ�ӵĵ��Ӳ���
��ͼ��������ͭ��Һ���Ȼ�����Һ��Ӧʾ��ͼ�������ӽǶȷ����û�ѧ��Ӧ�ܷ�����ԭ���� ��
��3�����Ʊ�������ƶԱ�ʵ����ʵ��̽������Ҫ������ 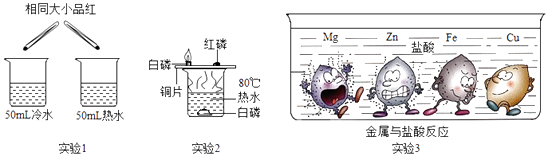
��ʵ��1��ͬʱ���ձ��м���һ����ͬ��С��Ʒ�죬��������ˮ����ʱ����ˮ����ˮ�̣�������Ϊ ��
��ʵ��2��ʹ��ͭƬ��Ϊ�˶Ա���ͬ��
��ʵ��3�Ǵ�С��״��ͬ��Mg��Zn��Fe��Cu���ֽ���ͬʱͶ�뵽�����з�������������Χ�ĺڵ��ʾ���ɵ����壮���н��۲���ȷ����������ĸ����
a��ͭ���ܷ����û���Ӧ
b�����ֽ����н��������ǿ����Mg
c����������п�����ֱ������������ᷢ����������������Zn��Fe�࣮
���𰸡�
��1���ų���������ˮ��FeO
��2��b�������Ӻ���������ӽ������������ˮ���ᱵ����
��3�����ȵ�����£��������������˶����ʼӿ죻��ȼ����Ż�㣻ac
���������⣺��1�������������ڵ�ȼ�������������������������ų��������ȣ�������Ʒ����ʴ���̣�ʵ��������������е�������ˮ�ȷ�����ѧ��Ӧ�Ĺ��̣�����FeSO4�������������ʾ��2�ۣ�����������ʾ+2�ۣ���������Ԫ�ػ��ϼ���ͬ������������Ļ�ѧʽ��FeO����2����ͼ��������������Ӧ�����Ȼ��Ƶ�ʾ��ͼ����ͼ˵���ڻ�ѧ��Ӧ�����У�ԭ�Ӻ˲��䣬���Ӳ������ܱ仯��ԭ���ڷ�����ѧ�仯ʱ��ͨ����ʧ�����γɻ��������һ�������仯����b��������ͭ���Ȼ�����Ӧ�������ᱵ�������Ȼ�ͭ�����Դ����ӽǶȷ����û�ѧ��Ӧ�ܷ�����ԭ���ǣ������Ӻ���������ӽ������������ˮ���ᱵ��������3���������¶ȿ��Լӿ���ӵ��˶����ʣ�����ʵ��1��ͬʱ���ձ��м���һ����ͬ��С��Ʒ�죬��������ˮ����ʱ����ˮ����ˮ�̣�������Ϊ�����ȵ�����£��������������˶����ʼӿ죻�ڰ����Ż��ͣ���ȼ�գ������Ż��ߣ���ȼ�գ�����ʵ��2��ʹ��ͭƬ��Ϊ�˶Աȿ�ȼ����Ż�㲻ͬ�����ڽ������˳���У�ֻ��������ǰ�Ľ����ſ��Ժ�ϡ����Һ��Ӧ��������������Խ��ǰ�Ľ�����Ծ�Խǿ����ϡ����Һ��Ӧʱ�����Խ���ң����� a��ͭ���ܷ����ᷢ����Ӧ��ͭ���Խ��������е����û����������Բ���˵ͭ���ᷢ���û���Ӧ���ʴ���
b��þ��������ݲ�������ң��������ֽ����н��������ǿ����Mg������ȷ��
c��ÿ65��������п������2��������������ÿ56����������������2�����������������Ե�������п�����ֱ������������ᷢ����������������Zn��Fe�٣��ʴ���
��ѡ��ac��
���Դ��ǣ���1���ٷų�����������ˮ����FeO����2����b���ڱ����Ӻ���������ӽ������������ˮ���ᱵ��������3�������ȵ�����£��������������˶����ʼӿ죻�ڿ�ȼ����Ż�㣻��ac��
�����㾫����������Ĺؼ���������������ϵ�ѡ�����ݵ����֪ʶ�����պ�ɫ������ͨ��ָ�����̡��������ǵĺϽ��ؽ�������ͭ��п��Ǧ�ȣ���ɫ��������������ơ�þ�����ȣ���ɫ������ͨ����ָ����ɫ��������������������Լ���ȼ����ȼ�յ����������⣬�˽�ȼ�յ���������ȱһ���ɣ���1����ȼ�2�����������������3���¶ȴﵽ�Ż�㣮


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��M�������г����Ľ�����MSO4��Һ����ɫҺ�壬ij��ѧ��ȤС���ͬѧ��̽��M��ͭ�����Ļ��˳�����������һ���������̽����� ��������⡿M��ͭ�����Ľ������˳���������ģ�
��1������������衿С���IJ�����Al��Cu��M��Сǿ�IJ�����Al��M��Cu����IJ����� �� �������ʵ�顿Ϊ��̽�����ֽ����Ļ��˳��ͬѧ��ȡ��ϸ��ͬ��M˿����˿�������Һ����������ͼ��ʾ��ʵ�飺
�۲쵽ֻ���Թ����з������Ա仯����ô�Թ����й۲쵽�������� ��
����������ͬѧ��һ����Ϊ�Թܱ���ҲӦ�������Ա仯��֮���Գ������������ԭ������� ��
����ͬѧ�Ƕ�ʵ������˸Ľ����Ѽס����е���˿��ĥ�ɾ����ֱַ����ԭ�Թ��У�����ס����Թ��ж����������Ա仯������Թ��з�����Ӧ�Ļ�ѧ����ʽΪ ��
��2������������ۡ�ͨ������ʵ�飬ͬѧ�ǵó������ֽ����Ļ��˳�� �������뷴˼��ʵ�������ͬѧ�Ƕ�ʵ����̽��������·�˼��
ͬѧ�Ǿ������ۺ���Ϊ��ʵ������Ż���ȥ���Թ������Թܱ�ţ��е�ʵ�飬Ҳ���Եó���ȷ�Ľ��ۣ�
��������ʵ���⣬�����Խ���˿��ͭ˿�ֱ���뵽ʢ����Һ���Թ��У�������һ�����ʣ��ֱ���뵽������������ͭ��Һ�У�����ʵ����������жϣ�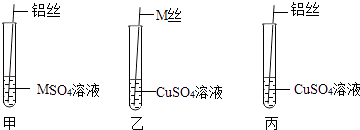
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ��һ�������в���ȱ�ٵ����ʣ����ۡ������������Լ���ԭ�������мв��е�ˮ����ʯ�ҽӴ�����Ӧ�ų������ȣ��÷�Ӧ�Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��P2O5�Ļ�ѧ�����ǣ� ��
A.��������
B.����������
C.���廯��
D.��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������غ㶨�ɵķ��ֶԻ�ѧ�ķ�չ�����˾��ף� 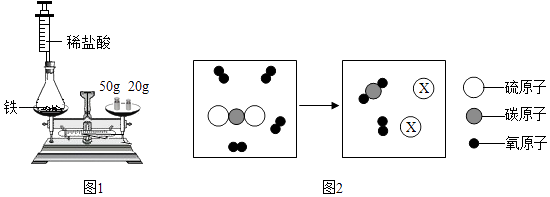
��1��Ϊ��֤�����غ㶨�ɣ�С�������ͼ1��ʾװ�ý���ʵ�飮 ʵ��ʱ���Ƚ�װ��ҩƷ��װ�÷�����ƽ�ϣ��������룬�ƶ���������ƽƽ�⣨��ͼ1��ʾ����Ȼ��ȡ��װ�ã�����Ͳ����ƿ��ע������ϡ���ᣬ��Ӧ���ٽ�װ�÷�������ƽ�ϣ��۲쵽 �� �Ӷ���֤�������غ㶨�ɣ�������ƿ��Ϊ�ձ���������֤�����غ㶨�ɣ�ԭ���� ��
��2��ij��Ӧ����ʾ��ͼ��ͼ2��ʾ�� ��X�Ļ�ѧʽ�� ��
�ڸ���������ʾ��ͼ���ɵó���ѧ��Ӧ��ѭ�����غ㶨�ɵı���ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л��ϳɲ��ϵij����Ƕ���Ȼ��Դ��һ�ֲ��䣬���в����в������л��ϳɲ��ϵ��ǣ� ��
A.����
B.����
C.�Ͻ�
D.�ϳ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com