
分析 (1)根据恰好使混合物完全溶解,说明反应后既没有固体,也没有盐酸,放出标准状况下的气体0.02克,说明有0.56g的Fe与盐酸反应,在溶液中,铁先与FeCl3反应再与HCl反应,说明溶液中不存在Fe3+,即只有Fe2+,即Fe3+全部与Fe反应,根据元素守恒可知铁元素的总质量;
(2)根据氧元素会与盐酸全部转化成水,所以金属氧化物减少的质量就是氧元素的质量.
解答 解:(1)根据题意,在溶液中,铁先与FeCl3反应再与HCl反应,可判断原混合物恰好溶于100克质量分数为3.65%的盐酸且反应后的溶液中无Fe3+存在,因此Fe元素在溶液中只以FeCl2的形式存在,溶液中氯离子与亚铁离子的个数比为2:1,
设铁的质量为x,
Fe------FeCl2-----2HCl
56 73
x 100g×3.65%
$\frac{56}{x}$=$\frac{73}{100g×3.65%}$
x=2.8g
故选:A;
(2)设减轻的质量为y
O------H2O-------2HCl
16 73
y 100g×3.65%
$\frac{16}{y}$=$\frac{73}{100g×3.65%}$
y=0.8g
故答案为:(1)A;
(2)0.8g.
点评 解答此题应抓着原混合物恰好溶于100克质量分数为3.65%的盐酸,且反应后的溶液中无Fe3+存在,即Fe元素只以FeCl2的形式存在.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
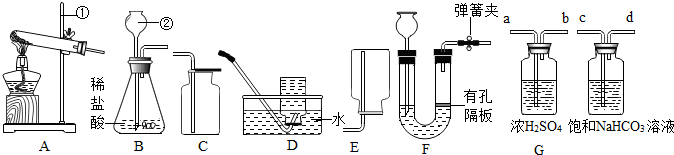
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质1 | 物质2 | |||||
| 选项 | 名称 | 化学式 | 物质类别 | 名称 | 化学式 | 物质类别 |
| A | 氢气 | H | 非金属单质 | 氧化铁 | Fe3O4 | 金属氧化物 |
| B | 硫酸钾 | K2SO4 | 盐 | 五氧化二磷 | P2O5 | 金属氧化物 |
| C | 汞 | HG | 金属单质 | 氢氧化镁 | Mg(OH)2 | 碱 |
| D | 碳酸氢钠 | NaHCO3 | 盐 | 硝酸 | HNO3 | 酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
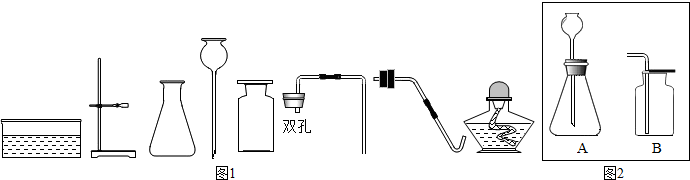
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 低温冷藏有利于减缓食品变质 | |
| B. | 食用碱可消除面粉发酵产生的酸味 | |
| C. | 蔬菜类食品焖熟,营养更丰富 | |
| D. | 保鲜膜可保持水果水分,隔绝空气,延长保质期 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 甲和乙两种物质的溶解度曲线如图所示:
甲和乙两种物质的溶解度曲线如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
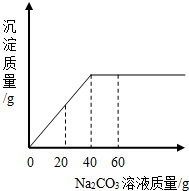 实验室有一瓶未知浓度的CaCl2溶液,某同学取出87g该溶液于烧杯中,向其中逐滴加入溶质质量分数为26.5%的Na2CO3溶液,反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图所示.
实验室有一瓶未知浓度的CaCl2溶液,某同学取出87g该溶液于烧杯中,向其中逐滴加入溶质质量分数为26.5%的Na2CO3溶液,反应过程中生成沉淀的质量与所用Na2CO3溶液质量的关系如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com