
分析 根据水是人体必需的营养素、硬水的概念、水的净化的程度进行分析解答;根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)水是人类所需的六大基本营养素之一,故填:属于.
(2)含有较多可溶性钙、镁化合物的水叫做硬水,故填:硬水.
(3)蒸馏是相对净化程度最高的净水方法,故填:C;
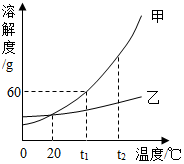
(4)①根据图示可以看出,在20℃时,甲和乙两种物质的溶解度相等,故填:20.
②甲的溶解度随温度的升高而变化明显,乙的溶解度随温度的升高变化不明显,故将t1℃时等质量的甲和乙两种物质的饱和溶液分别降温到0℃,析出固体质量较少的是乙,故填:乙.
③t2℃时,加的溶解度大于60g,乙的溶解度小于60g,故将60g甲物质放入100g水中,充分搅拌,所得溶液的溶质质量分数w(甲)与同温下乙物质的饱和溶液的溶质质量分数w(乙)大小关系为w(甲)>w(乙),故填:B.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:初中化学 来源: 题型:推断题
 A、B、C、D、E、F、G是中学化学常见物质,A、B均为金属氧化物,A与常见无色液体F反应生成C,同时放出大量的热,E是蓝色沉淀,它们的转化关系如图所示(部分生成物略去).
A、B、C、D、E、F、G是中学化学常见物质,A、B均为金属氧化物,A与常见无色液体F反应生成C,同时放出大量的热,E是蓝色沉淀,它们的转化关系如图所示(部分生成物略去).查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 2014年初,电视剧《来自星星的你》风靡亚洲,也在我国刮起一股“韩流”,带动了很多产品的热销.
2014年初,电视剧《来自星星的你》风靡亚洲,也在我国刮起一股“韩流”,带动了很多产品的热销.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红磷在空气中燃烧产生大量白色烟雾 | |
| B. | 细铁丝在空气中剧烈燃烧,火星四射,生成黑色固体 | |
| C. | 镁条放入稀盐酸中,反应后溶液温度升高 | |
| D. | 电解水实验中,正极产生的气体能燃烧 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 4.8g | B. | 3.4g | C. | 3.2g | D. | 2.4g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com