

分析 根据人体所需的营养素的主要来源和食物中富含的营养素进行分析;根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析.
解答 解:(1)小麦粉中富含淀粉;
(2)食用植物油中富含油脂;
(3)维生素D属于维生素;
(4)全脂奶粉中含有丰富蛋白质;
(5)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
故答案为:(1)小麦粉;(2)食用植物油;(3)维生素D;(4)全脂奶粉;(5)CaCO3+2HCl=CaCl2+H2O+CO2↑.
点评 本题难度不大,掌握人体所需的营养素的主要来源和食物中富含的营养素及化学方程式的书写是解答此题的关键.


科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 炒菜的油锅起火,可用锅盖盖灭 | |
| B. | 图书档案起火,可用水浇灭 | |
| C. | 酒精灯不慎打翻起火,可用湿抹布扑灭 | |
| D. | 森林、草场引起火灾,应设置隔离带 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 某同学绘制了如图所示A、B两种固体物质的溶解度曲线,请回答下列问题:
某同学绘制了如图所示A、B两种固体物质的溶解度曲线,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 某无色溶液可能含有NaOH、HCl、H2SO4、NaCl、Na2CO3、MgCl2、FeCl3中的一种或几种,加入氢氧化钡溶液,产生沉淀与加入的氢氧化钡溶液量的关系如图:
某无色溶液可能含有NaOH、HCl、H2SO4、NaCl、Na2CO3、MgCl2、FeCl3中的一种或几种,加入氢氧化钡溶液,产生沉淀与加入的氢氧化钡溶液量的关系如图:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
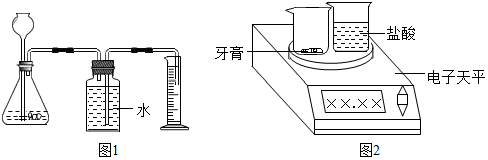
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Ca(OH)Cl | B. | Ca(HCO3)2 | C. | Ca2(OH)2CO3 | D. | Ca(OH)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
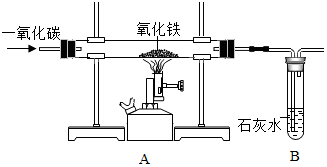 某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物.所用装置如图所示.
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe2O3反应后的产物.所用装置如图所示.| 玻璃管中固体的质量 | 装置B试管及其中物质的总质量 | |
| 反应前 | 32g | 300g |
| 反应后 | 28.8g | 308g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com