
 ,则X是(写化学式).若用废铜屑、稀硫酸和空气作原料制取硫酸铜,依次写出制备过程中发生反应的化学方程式,.
,则X是(写化学式).若用废铜屑、稀硫酸和空气作原料制取硫酸铜,依次写出制备过程中发生反应的化学方程式,. 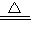 2CuO;CuO+H2SO4═CuSO4+H2O.
2CuO;CuO+H2SO4═CuSO4+H2O.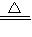 2CuO;CuO+H2SO4═CuSO4+H2O.
2CuO;CuO+H2SO4═CuSO4+H2O.

科目:初中化学 来源: 题型:
| O2加热 |
| 浓硫酸 |
| 浓硫酸 |
| ||
| FeSO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:022
(2005
年山西)废铜屑与浓硫酸反应,能制得硫酸铜,其反应原理是: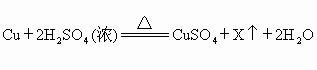
查看答案和解析>>
科目:初中化学 来源:2005年山东省潍坊市中考化学试卷(课改区)(解析版) 题型:填空题

查看答案和解析>>
科目:初中化学 来源:2005年各省市中考化学汇编:探究题选(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com