
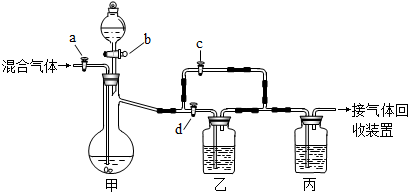
分析 根据二氧化碳与一氧化碳均属气体,分离时应该用化学方式先反应掉一种物质,得到一种物质后,再把第一种物质从一些物质中制取出来进行分析.
解答 解:(1)氢氧化钠会与二氧化碳反应生成碳酸钠,碳酸钠和硫酸反应会生成二氧化碳,浓硫酸有吸水性,所以甲、丙两装置中盛放的分别是氢氧化钠溶液、浓硫酸,打开活塞a、d,关闭活塞b、c,通入混合气体后,氢氧化钙和二氧化碳反应会生成碳酸钙沉淀和水,若乙装置中的现象是溶液不变浑浊,说明甲装置中反应充分,此步实验后收集到的气体是一氧化碳;
(2)在甲装置的分液漏斗中加入试剂稀硫酸或稀盐酸,关闭活塞b、c,打开活塞a、d,再经过丙装置后即可收集到另一种气体.此步实验中发生的反应是碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,碳酸钠和硫酸反应生成硫酸钠、水和二氧化碳,化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑或Na2CO3+H2SO4=Na2SO4+H2O+CO2↑.
故答案为:(1)氢氧化钠溶液、浓硫酸,溶液不变浑浊,一氧化碳;
(2)Na2CO3+2HCl═2NaCl+H2O+CO2↑或Na2CO3+H2SO4=Na2SO4+H2O+CO2↑.
点评 本题考查了一氧化碳与二氧化碳的分离方式,实际上是先通过试剂除掉一种物质,而后再把吸收后的物质与其他物质反应制取出开始除掉的物质.


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:初中化学 来源: 题型:选择题
| A. | 纯净物一定由同种元素组成,混合物一定由不同种元素组成 | |
| B. | 化学反应的过程,会发生原子的重新组合 | |
| C. | 磷元素和硅元素本质区别是它们原子核内的质子数不同 | |
| D. | 铁、氢气、氯化钾分别是由由原子、分子、离子构成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 铁、氯化铜、石灰水、稀盐酸、石灰石之间的反应关系如图所示,图中两圆相交部分(a、b、c、d)表示物质间反应的类型或主要实验现象.下列说法中错误的是( )
铁、氯化铜、石灰水、稀盐酸、石灰石之间的反应关系如图所示,图中两圆相交部分(a、b、c、d)表示物质间反应的类型或主要实验现象.下列说法中错误的是( )| A. | a处产生红色物质 | B. | b处生成没有明显现象 | ||
| C. | c处发生复分解反应 | D. | d处产生气泡 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
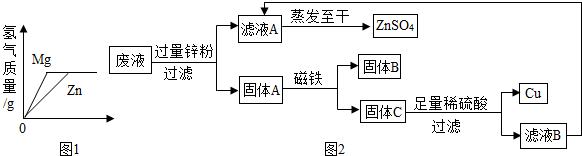
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | a-b-c-d | B. | b-a-c-d | C. | b-d-c-a | D. | b-d-a-c |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
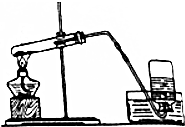 如图是实验室里用高锰酸钾制取氧气的装置图,该装置图中的错误是( )
如图是实验室里用高锰酸钾制取氧气的装置图,该装置图中的错误是( )| A. | 试管口略向上倾斜 | B. | 用排水法收集 | ||
| C. | 集气瓶中导管太短 | D. | 试管中导管伸入过长 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com