
分析 硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,根据反应的化学方程式和提供的数据可以进行相关方面的计算.
解答 解:(1)设硫酸铜质量为x,生成沉淀氢氧化铜质量为y,
反应的氢氧化钠质量为:Wg×40%=0.4Wg,
2NaOH+CuSO4═Na2SO4+Cu(OH)2↓,
80 160 98
0.4Wg x y
$\frac{80}{0.4Wg}$=$\frac{160}{x}$=$\frac{98}{y}$,
x=0.8Wg,y=0.49Wg,
0.4Wg氢氧化钠在钠元素质量为:0.4Wg×$\frac{23}{40}$×100%=0.23Wg,
Wg氢氧化钠溶液中钠元素的质量分数为:$\frac{0.23Wg}{Wg}$×100%=23%,
答:Wg氢氧化钠溶液中钠元素的质量分数为23%.
(2)根据质量守恒定律可知,硫酸铜溶液质量为:2.51Wg+0.49Wg-Wg=2Wg,
所加硫酸铜溶液中溶质质量分数为:$\frac{0.8Wg}{2Wg}$×100%=40%,
答:所加硫酸铜溶液中溶质质量分数为40%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 向硬水中加明矾净水剂后得到纯水 | |
| B. | 水中N、P元素超标会导致水体富营养化 | |
| C. | 用渗透膜淡化海水是分子运动的结果 | |
| D. | 工业废水可先循环使用再净化 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 青菜 | B. | 牛奶 | C. | 炒花生 | D. | 玉米 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
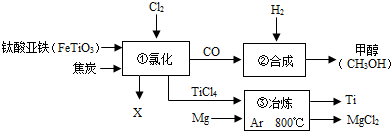
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 发生装置 | 收集装置 | 吸气装置 |
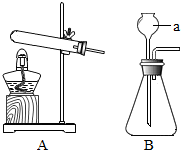 | 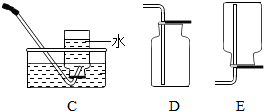 | 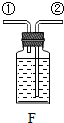 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
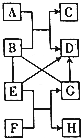 A--H是初中化学常见的物质,它们能相互转化关系如图所示,图中“→”表示转化关系,“-”表示相互能反应(部分物质和反应条件为标出).已知D是人体中含量最多的物质,F可用于改良酸性土壤,且与G属于同类
A--H是初中化学常见的物质,它们能相互转化关系如图所示,图中“→”表示转化关系,“-”表示相互能反应(部分物质和反应条件为标出).已知D是人体中含量最多的物质,F可用于改良酸性土壤,且与G属于同类查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 冬天取暖时,室内放一定量的水可以防煤气中毒 | |
| B. | 高温下,利用一氧化碳把铁从铁矿石中还原出来 | |
| C. | 废旧纸张、易拉罐和塑料瓶放入可回收垃圾箱 | |
| D. | 过滤时,用玻璃棒引流 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 /g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCl | 35.7 | 36 | 36.6 | 37.3 | 38.4 | 39.8 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com