
| A. | 碳酸钠10g、碳酸钙10g | B. | 铁5.6g、锌5.6g | ||
| C. | 铁8.0g、氧化铜8.0g | D. | 碳酸钙10g、碳酸镁10g |
分析 因为加入的盐酸质量相等,所以需要判断两端加入一定量物质后增加质量是否相等,增加质量相等时天平能仍然保持平衡,不相等时天平发生偏转.可根据化学方程式,借助关系式和差量法进行分析比较.
解答 解:100g 7.3%的稀盐酸中HCl质量=100g×7.3%=7.3g
A、CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73
由化学方程式可知,10g的碳酸钠、碳酸钙与盐酸可反应生成的二氧化碳的质量不同,天平不平衡,故A错误;
B、100g 7.3%的稀盐酸完全反应消耗金属铁和锌的质量分别为:
Fe~2HCl
56 73
m(Fe) 7.3g
$\frac{56}{73}=\frac{m(Fe)}{7.3g}$ 解之得 m(Fe)=5.6g
Zn~2HCl
65 73
m(Zn ) 7.3g
$\frac{65}{73}=\frac{m(Zn)}{7.3g}$ 解之得 m(Zn)=6.5g
则金属铁与稀盐酸恰好反应完,锌与盐酸反应,盐酸有剩余,所以铁与盐酸反应放出氢气质量多,天平不平衡,不B错误;
C、铁和盐酸反应放出氢气,而氧化铜和盐酸反应不会放出气体,
100g7.3%的稀盐酸完全反应消耗铁条的质量分别为x,生成氢气的质量为y
Fe~2HCl~H2
56 73 2
x 7.3g y
$\frac{56}{x}=\frac{73}{7.3g}=\frac{2}{y}$ 解得:x=5.6g y=0.2g
铁和盐酸恰好完全反应,烧杯质量增加了:8g-0.2g=7.8g,
而氧化铜和盐酸反应不放出气体,所以增加8g,所以天平不包平衡,故C错误.
D、CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73
MgCO3+2HCl=MgCl2+H2O+CO2↑
84 73
由化学方程式可知,10g的碳酸钙、碳酸镁与盐酸可反应生成的二氧化碳的质量相同,天平平衡,故D正确.
故选:D.
点评 加入物质充分反应后,天平一端增加的质量=加入固体质量-放出气体的质量,只有加入物质与放出气体质量均相等时,天平才能保持平衡.由于运算量比较大,所以对于有关化学方程式的计算是否熟练是解题的关键.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
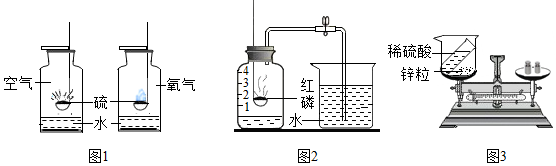
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na2SO4+2KCl═K2SO4+2NaCl | B. | 2Fe+6HCl═2FeCl3+3H2↑ | ||
| C. | Cu+MgSO4═CuSO4+Mg | D. | Na2CO3+CaCl2═CaCO3↓+2NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象.实验结论 | |
| 1、取适量黑色滤渣装入试管中,再加入过量稀盐酸 | 无气泡生成,溶液不变色 | 黑色粉末中一定不含铁粉与氧化铜 |
| 2、取适量黑色滤渣装入另一支试管中,再加入H2O2(或过氧化氢)溶液,向上述试管中伸入带火星的小木条. | 木条复燃 | 黑色粉末中含有二氧化锰 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
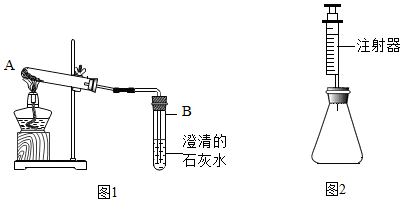
| 实验编号 | 锥形瓶内物质[来源 | 最终得到 CO2 体积/mL | |
| 名称 | 质量/g | ||
| ① | 碳酸钠 | a | V1 |
| ② | 碳酸氢钠 | a | V2 |
| ③ | 白色粉末 | m | V3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用互相刻画的方法,可比较硬铝和铝的硬度 | |
| B. | 用熟石灰粉末研磨,可鉴别硫酸铵和氯化铵 | |
| C. | 用灼烧闻气味的方法,可区分棉纤维和羊毛 | |
| D. | 用带火星的木条,可鉴别氧气和空气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com