
【题目】能保持水的化学性质的微粒是 ( )
A. 氧原子 B. 氢分子 C. 水分子 D. 氧原子和氢原子
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:初中化学 来源: 题型:
【题目】某化学兴趣小组利用下图装置进行实验。探究工业炼铁的化学原理,试按要求填空。

(1)硬质玻璃管中观察到的现象是__________,写出一氧化碳和氧化铁反应的化学方程式________;
(2)实验中首先通入一氧化碳的目的是__________;
(3)装置中导管末端加一点燃的酒精灯目的是______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将50g石灰石放入烧杯中,加入100g稀盐酸恰好完全反应(杂质不溶解,也不参加反应),此时,烧杯中物质的总质量为141.2g
(1)石灰石中碳酸钙的质量分数是多少?
(2)所用盐酸的溶质质量分数是多少?
(3)反应后,过滤所得溶液的溶质质量分数是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】t2 ℃时,将甲,乙各80 g分别放到盛有100 g水的两个烧杯中,充分溶解后,恢复到t2 ℃,现象如图一。甲和乙的溶解度曲线如图二。请结合图示回答下列问题:

(1)固体甲对应的溶解度曲线是________(填“a”或“b”)。
(2)M点的含义________________________________________。
(3)向烧杯①的溶液中继续加入15 g甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分固体甲析出。你认为“全部溶解”的原因是______________________________________。
(4)将t2 ℃等质量的甲、乙饱和溶液分别降温到t1 ℃时,所得溶液的有关说法正确的是________(填字母)。
a.甲溶液仍为饱和溶液
b.两溶液质量甲<乙
c.两溶液中溶剂质量甲=乙
d.两溶液溶质质量甲>乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图为甲、乙两种物质的溶解度曲线。
资料:常温(20 ℃)下,溶解度的相对大小。
溶解度/g | <0.01 | 0.01~1 | 1~10 | >10 |
一般称为 | 难溶 | 微溶 | 可溶 | 易溶 |
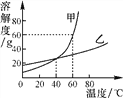
(1)常温下,乙属于________(填“易溶”“可溶”“难溶”或“微溶”)物质。
(2)________ ℃时,甲、乙两种物质的溶解度相等。
(3)60 ℃时,甲饱和溶液中溶质的质量分数为________。
(4)把60 ℃时质量相等的甲、乙饱和溶液降温到20 ℃,析出晶体较多的物质是________。
(5)要使乙的饱和溶液中溶质大量结晶析出,应该采用________的方法。
(6)若要从甲、乙的混合溶液中提纯甲,则主要操作是蒸发浓缩、________、________、干燥。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向160g硫酸铜溶液中,逐滴加入40g NaOH溶液,恰好完全反应,生成4.9g沉淀,回答下列问题:

(1)恰好完全反应后,溶液的质量为 g。
(2)将反应结束后的混合物过滤,滤液中溶质是 (填化学式)。
(3)求原硫酸铜溶液中溶质的质量分数(写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化工生产中需要对原料提纯,以利于提高产品质量。经测定某氯化钠样品中混有硫酸钠,为了除杂质并制得纯净的氯化钠固体,在实验室研究中某学生设计方案如下:
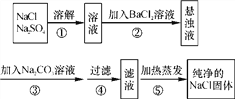
回答下列问题。
(1)操作②能否用硝酸钡溶液?说明理由。________________________________________。
(2)进行操作②后,如何判断硫酸钠已除尽,方法是_____________________________________________________。
(3)操作③的目的是________________,③、④的操作顺序能否交换,其理由是________________。
(4)此设计方案是否严密,说明理由__________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com