
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题

 .
.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 图中A-I表示几种初中化学常见的物质,“→”表示物质间存在相应的转化关系,部分反应物、生成物及反应条件已略去.已知圈Ⅰ中转化均是分解反应,圈Ⅱ中的转化均是化合反应,D和G是常见的非金属单质,组成化合物E和H的元素种类相同,组成化合物F和I的元素种类也相同,A常用来中和土壤的酸性.
图中A-I表示几种初中化学常见的物质,“→”表示物质间存在相应的转化关系,部分反应物、生成物及反应条件已略去.已知圈Ⅰ中转化均是分解反应,圈Ⅱ中的转化均是化合反应,D和G是常见的非金属单质,组成化合物E和H的元素种类相同,组成化合物F和I的元素种类也相同,A常用来中和土壤的酸性.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 稀盐酸中能解离出氢离子,硫酸溶液中也能解离出氢离子 | |
| B. | 铝锅表面易形成致密的氧化铝薄膜耐腐蚀,铁制品表面易形成铁锈也耐腐蚀 | |
| C. | 某石灰矿中检测出含有氧化铁,因此该矿石也可用来炼铁 | |
| D. | 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
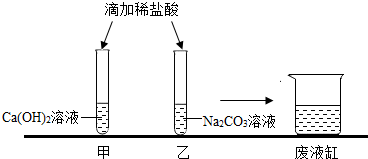
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com