(2013?白云区一模)为了维护南海权益,我国去年宣布成立了三沙市.这是维护国家主权的象征,同时也是因为海洋资源十分丰富,有广泛的利用价值.其中通过海水晾晒即可得粗盐,粗盐除NaCl外,还含有MgCl
2、CuCl
2、Na
2SO
4以及泥沙等杂质.以下是制备精盐的实验方案,各步操作流程如下:
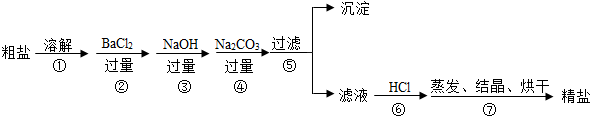
(1)根据以上信息,请写出海水中所含的主要阴离子的符号
Cl-、SO42-
Cl-、SO42-
.
(2)在上述流程中第③步加过量NaOH的目的是除去海水中的
Mg2+
Mg2+
(填离子符号,下同),第④步加过量Na
2CO
3的目的是除去海水中的
Ba2+、Cu2+
Ba2+、Cu2+
.第⑥步其实显示的是加适量盐酸,其目的是除去多余的
OH-、CO32-
OH-、CO32-
.
(3)请写出第②步所发生反应的化学方程式
Na2SO4+BaCl2=BaSO4↓+2NaCl.
Na2SO4+BaCl2=BaSO4↓+2NaCl.
.
(4)在第③步操作中,选择的除杂试剂不能用KOH代替NaOH,理由是
如果用KOH代替NaOH,最得到的精盐中含有氯化钾.
如果用KOH代替NaOH,最得到的精盐中含有氯化钾.
.



